证明Al2O3具有两性的反应事实是______________________(用离子方程式表示)。
某溶液中可能含有Cl-、I-、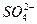 、
、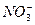 、
、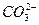 、
、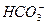 ,现进行如下实验:
,现进行如下实验:
(1)取部分溶液,加入过量Ba(NO3)2溶液,有白色沉淀生成,过滤出的沉淀部分溶于稀HNO3,并放出气体。
(2)取部分滤液,加入过量NaOH溶液,无沉淀产生。
(3)取部分滤液,加入AgNO3溶液,只有黄色沉淀生成。
根据上述现象,试判断:溶液中肯定存在的离子是____________,肯定不存在的离子是____________,可能存在的离子是____________。
在下图所示的转化关系中,已知B、D都是淡黄色固体,A与D反应生成离子化合物,完成下列问题。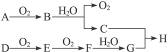
(1)写出下列物质的化学式:A.__________;F. __________;H. __________。
(2)写出C的电子式:____________________。
(3)写出B C,E
C,E F的化学方程式:___________________________________。
F的化学方程式:___________________________________。
对绿矾晶体加强热,全部反应后将生成的混合气体通入浓BaCl2溶液中,生成硫酸钡白色沉淀,同时放出能使品红溶液褪色的气体,过滤沉淀后得浅黄色溶液。试写出绿矾晶体分解的化学方程式。最后获得的浅黄色溶液中所含的溶质有。
从某物质A的水溶液出发有下图所示的一系列变化: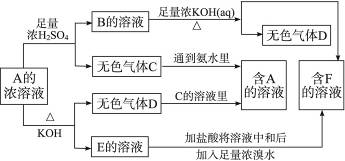
试完成下列问题:
(1)物质的化学式:A____________,B____________,C____________,D____________,E____________,F____________。
(2)写出EF的离子方程式________________________。
(3)鉴定物质F的方法________________________。
在下列反应中:
2FeO+4H2SO4(浓)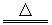 Fe2(SO4)3+SO2↑+4H2O
Fe2(SO4)3+SO2↑+4H2O
H2SO4表现出的性质是____________,FeO表现出的性质是____________;该反应的氧化产物和还原产物的物质的量之比是____________。