铬铁矿的主要成分可表示为FeO·Cr2O3,还含有SiO2、Al2O3等杂质,以铬铁矿为原料制备重铬酸钾(K2Cr2O7)的过程如下图所示。
已知:① NaFeO2遇水强烈水解。 ② Cr2O72-+ H2O 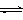 2CrO42- + 2H+
2CrO42- + 2H+ K2Cr2O7中Cr元素的化合价是 。
K2Cr2O7中Cr元素的化合价是 。
生成滤渣1中红褐色物质反应的化学方程式是 。
滤液1的成分除Na2CrO4、Na2SiO3外,还含有(填化学式) 。
利用滤渣2,可制得两种氧化物,其中一种氧化物经电解冶炼可获得金属,该电解反应的化学方程式是 。
由滤液2转化为Na2Cr2O7溶液应采取的措施是 。
向Na2Cr2O7溶液中加入KCl固体,获得K2Cr2O7晶体的操作依次是:加热浓缩、 、过滤、洗涤、干燥。
煅烧铬铁矿生成Na2CrO4和NaFeO2反应的化学方程式是 。
A、B、C、D、E代表5种元素。请填空:
(1)A元素基态原子的最外层有3个未成对电子,次外层有2个电子,其元素符号为;
(2)B元素的负一价离子和C元素的正一价离子的电子层结构都与氩相同,B的元素符号为,C的元素符号为;
(3)D元素的正三价离子的3d亚层为半充满,D的元素符号为,其基态原子的电子排布式为。
(4)E元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,E的元素符号为,其基态原子的电子排布式为。
(12分)依据氧化还原反应:2Ag+(aq)+Cu(s) = Cu2+(aq)+2Ag(s)设计的原电池如图所示。请回答下列问题: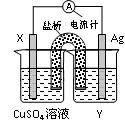
(1)电极X的材料是________;电解质溶液Y是___________;
(2)银电极为电池的________极,
发生的电极反应为______________________________;
X电极上发生的电极反应为____________________________;
(3)外电路中的电子是从_______电极流向________电极。
已知F为高分子化合物: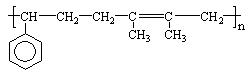
C分子结构中只含有一种氢。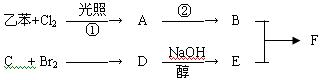
(1)写出下列物质结构简式
A:C:E:
(2)判断①反应类型:
(3)写出②反应进行所需条件:
(4)写出C7H80所有含苯环结构的同分异构体:(提示:5种同分异构体)
丙烯是石油化工的重要原料,一定条件下可发生下列转化:
已知: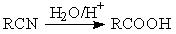

(1)A的结构简式为:____________;
(2)反应④的类型为:_________________反应;
(3)D与足量乙醇反应生成E的化学方程式为:______________________________。
(4) 与足量NaOH溶液反应的化学方程式为____________________。
与足量NaOH溶液反应的化学方程式为____________________。
(5)B的同分异构体有多种.写出其中既能发生银镜反应,又能发生酯化反应的2种同分异构体的结构简式:_______________、___________________。
已知丙烯与水进行加成反应,其可能的产物有两种:(2)下图中E为开链的酯类化合物,其分子式为C6H12O2
请依据上述条件和图中转化关系,在方框中填入合适的化合物的结构简式。