实验室欲配制0.5 mol/L的NaOH溶液500 mL,有以下仪器:①烧杯 ②玻璃棒 ③托盘天平(带砝码) ④药匙,按要求填空:
(1)配制时,需称取NaOH的质量是 g,还缺少的仪器是
。
(2)使用容量瓶前必须进行的一步操作是 。
(3)在配制过程中,其他操作都正确的情况下,下列操作会导致所配制的溶液浓度偏高的是 。(选填序号)
①没有洗涤烧杯和玻璃棒 ②未等NaOH溶液冷却至室温就转移到容量中
③容量瓶不干燥,含有少量蒸馏水 ④定容时仰视标线 ⑤定容时俯视标线
某白色粉末其成分可能是碳酸钠和亚硫酸钠的一种或两种组成。请完成对该白色粉末成分的探究:
限选实验仪器:药匙、试管、单孔塞、导管、玻璃棒、滴管、带铁夹的铁架台。
限选实验试剂:1 mol·L-1H2SO4、3%H2O2、澄清石灰水、品红试液。
(1)提出合理假设
假设1:该白色粉末成分为亚硫酸钠;
假设2:该白色粉末成分为碳酸钠;
假设3: 。
(2)设计实验方案证明(1)的假设
(3)实验过程
根据(2)的实验方案,进行实验。写出实验操作步骤、预期现象与结论。
| 实验操作 |
预期现象与结论 |
| 步骤1:检查装置气密性(略) |
|
| 步骤2: |
|
| 步骤3: |
下图是实验室用来验证乙烯与氢气反应产物的装置,请回答下列问题: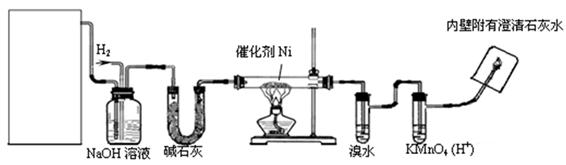
(1)方框内装置用来制取乙烯,现有下列仪器及用品:①碎瓷片②石棉网和铁架台③圆底烧瓶④温度计(量程100℃)⑤温度计(量程200℃)⑥酒精灯⑦单孔塞⑧双孔塞⑨导管。
其中不需用的仪器及用品有(填序号)
(2)写出制乙烯化学方程式:
(3)碱石灰的作用是:
(4)溴水的作用是:
(5)出现什么现象可说明生成了乙烷?
油条是一种深受群众喜爱的传统食品,在百姓早餐桌上一直占有重要位置。但油条中铝含量超标问题十分普遍,是影响群众健康的食品安全隐患。从2009年5月下旬开始,浙江省的油条加工停用含铝食品的添加剂,逐步转换为无铝添加剂配方和工艺,从而保证百姓吃上安全、放心的油条。油条无铝配方由碳酸氢钠(小苏打)、碳酸氢铵(臭粉)组成。为测定试样中WWW.K**S*858$$U.COM小苏打的质量分数w(NaHCO3),实验小组同学设计了如下装置进行实验。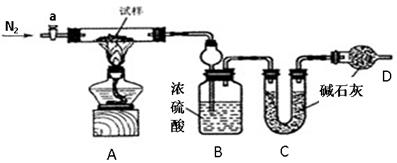
实验过程:
①按图组装仪器,检查装置的气密性;
②将试样m1g放入硬质玻璃管中,装置B、C、D中药品如图,已知加药品后装置B的质量
为m2g、装置C的质量为m3g;
③打开活塞a,通N2一段时间后,关闭活塞a,点燃酒精灯加热试样,直到B装置中无气泡冒出后,打开活塞a向装置中通入N2,一段时间后,撤掉酒精灯,关闭活塞a;
④称得装置B的质量为m4g、装置C的质量为m5g。
请回答以下问题:
(1)装置A中发生反应的化学方程式为,
。
(2)装置D的作用为防止空气中进入装置C中。
装置C的作用为。
(3)实验过程中第二次通入N2的目的是把装置中产生的排出,使其被装置B和装置C完全吸收。
(4)用下列各项所提供的数据能计算出w(NaHCO3)的是()(填写序号)
| 序号 |
a |
b |
c |
d |
e |
| 数据 |
m1、m2、m3 |
m2、m3、m4、m5 |
m1、m2、m4 |
m1、m4、m5 |
m1、m3、m5 |
(5)实验结束后发现装置A中硬质玻璃管右端有水珠,你认为利用实验中所提供的数据还能否得到准确的w(NaHCO3)(填“能”或“不能”)。
某化学小组利用浓盐酸和二氧化锰在加热条件下制取氯气,并利用氯气进行有关的探究实验 ,制取氯气的装置如图I和Ⅱ。
,制取氯气的装置如图I和Ⅱ。
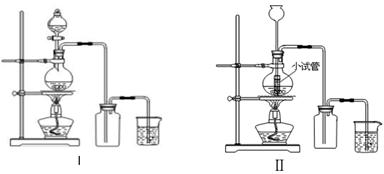
(1)制取氯气的反应的离子方程式;
(2)装置Ⅱ中小试管的作用为;
(3)装置I与装置Ⅱ比较,装置I的主要优点为:。
(4)将生成的氯气通入水中,可制得氯水,氯水见光易分解生成气体。
(5)氯气能使湿润的红色布条褪色。对于使红色布条褪色的物质,同学们的看法不一致,认为氯水中存在的几种粒子都有可能,请利用中学实验室常见试剂,设计实验,得出正确结论。
| 提出问题 |
收集资料 |
提出假设 |
验证假设 |
得出结论 |
| 氯水中何种物质能使湿润的红色布条褪色? |
①Cl2有强氧化性 ②Cl2与冷水反应生成盐酸和HClO ③HClO有强氧化性 |
①。 ②盐酸使布条褪色。 ③。 ④H2O使布条褪色 |
验证假设①:把红色干布条放入充Cl2的集气瓶,布条不褪色; 验证假设②:。 验证假设④:把红色布条放在水里,布条不褪色。 |
使红色布条褪色的物质是。 |
配制一定物质的量浓度溶液是一个重要的定量实验。请回答以下问题:
(1)要配制浓度约为2 mol·L-1的NaOH溶液100mL,下列操作正确的是
A.称取8gNaOH固体,放入250mL烧杯中,用量筒量取100mL蒸馏水,加入烧杯中,同时不断搅拌至固体溶解
B.称取8gNaOH固体,放入100mL量筒中,边搅拌,边慢慢加入蒸馏水,待固体完全溶解后用蒸馏水稀释至100mL
C.称取8gNaOH固体,放入100mL容量瓶中,加入适量蒸馏水,振荡容量瓶使固体溶解,再加水至刻度线WWW.K**S*858$$U.COM,盖好瓶塞,反复摇匀
D.用100mL量筒称取40mL 5mol·L-1的NaOH溶液,倒入250mL烧杯中,再用同一量筒量取60mL蒸馏水,不断搅拌下,慢慢倒入烧杯中
(2)下列操作使配制的BaCl2溶液浓度偏低的是
A.未洗涤烧杯和玻璃棒 B.选用的容量瓶内有少量蒸馏水
C.有少量洗涤液未能全部转移到容量瓶中
D.定容摇匀后,液面下降,又加水至刻度线
(3)某实验中需要2mol·L-1的Na2CO3溶液950mL,配制时应选用容量瓶的规格为,称取固体Na2CO3的质量为。