X、Y、Z、W是元素周期表前四周期中常见的元素,其相关信息如下表:
| 元素 |
相关信息 |
| X |
X的基态原子L层电子数是K层电子数的2倍 |
| Y |
Y的基态原子最外层电子排布式为:nsnnpn+2 |
| A |
Z存在质量数为23,中字数为12的核素 |
| W |
W有多种化合价,其白色氢氧化合物在空气中会迅速变成灰绿色,最后变成红褐色 |
(1)W的原子结构示意图为________。
(2)X的电负性比Y的____________(填“大”或“小”);X 和Y的气态氢化物中,较稳定的是______________(写化学式)。
(3)写出Z2Y2与XY2反应的化学方程式:________________.
(4)在X的原子和氢原子形成的多分子中,有些分子的核磁共振氢谱显示两种氢,写出其中一种分子的名称:____________。氢元素,X、Y的原子也可共同形成多种分子和几钟常见无机阴离子,写出其中一种分子与该无机阴离子反应的离子方程式:_______________。
烷基的通式__________,甲基的电子式__________,乙烷的电子式__________,分子式为CmH20的烷烃中m为__________,分子式为C8Hn的烷烃中n为__________,与CO2密度相同(同温同压)的烷烃分子式为__________。
乙烷和丙烷的混合气体完全燃烧后,产物依次通过足量的浓硫酸和过氧化钠,它们分别增重2.04g和2.24g。则乙烷和丙烷的体积比是__________。
有下列各组物质,请按要求填入序号:
A.O2和O3(臭氧)
B.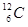 和
和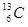
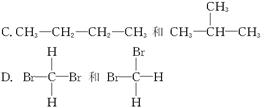
E.甲烷和庚烷
①____________组两物质互为同位素。
②____________组两物质互为同素异形体。
③____________组两物质属于同系物。
④____________组两物质互为同分异构体。
⑤____________组中的物质是同一物质。
相对分子质量为72的烷烃,其分子式是________。若此有机物的一氯代物分子中有两个—CH3,两个—CH2—,一个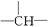 和一个—Cl,它的可能结构分别是________、____________、____________、____________。
和一个—Cl,它的可能结构分别是________、____________、____________、____________。
T℃时,将3mol气体A和1mo1气体B通入容积为2L且固定不变的密闭容器中,发生如下反应:3A(g)+B(g) 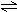 xC(g),2min时反应达到平衡状态(温度不变),此时容器内剩余了0.8molB,并测得C的浓度为0.4mol/L。请填写下列空白:
xC(g),2min时反应达到平衡状态(温度不变),此时容器内剩余了0.8molB,并测得C的浓度为0.4mol/L。请填写下列空白:
(1)从反应开始到平衡状态,生成C的平均速率为;X=;
(2)若向原平衡混合物的容器中再充入amolC,在T℃达到新的平衡,此时B的物质的量为n(B)=;
(3)保持温度和容积不变,对原平衡混合物中三者的物质的量作如下调整,可使平衡
向右移动的是;
A.均减半 B.均加倍 C.均增加0.4mol D.均减少0.4mol
(4)若上述可逆反应的热化学方程式为:
3A(g)+B(g) 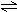 xC(g) ;△H =-QKJ/mol (Q>0)
xC(g) ;△H =-QKJ/mol (Q>0)
①若可逆反应达到平衡后升高体系温度,正反应速率(填“增大”、“减小”或“不变”),平衡将(填“左移”、“右移”或“不移动”)
②若可逆反应达到平衡后增大压强,则体系温度将(填“升高”、“降低”或“不变”)
③若可逆反应达到平衡后,加入A,则△H(填“变大”、“变小”或“不变”