如何除去下列物质中所含少量的杂质?写出所需试剂、分离方法及所用仪器。
| 混合物 |
所用试剂 |
分离方法 |
使用仪器 |
| ①肥皂水(甘油) |
|
|
|
| ②乙酸乙酯(乙酸) |
|
|
|
| ③硬脂酸(硬脂酸钠) |
|
|
|
根据要求填空:
(1)根据要求写出下列反应的化学方程式:
①有水参加的置换反应,承作氧化剂
②有水参加的氧化还原反应,水既是氧化剂又是还原剂。
③有水参加的氧化还原反应.但水既不是氧化剂又不是还原剂。
④有水参加的复分解反应。
(2)“绿色试剂”双氧水可作为矿业废渣消毒剂,消除采矿业艘液中的氰化物(如KCN)的化学方程式为:KCN+H2O2+H2O=A+NH3↑
①生成物A的化学式为。
②在标准状况下有0.448L氨气生成.则转移的电子数为。
③反应中被氧化的元素为。
(3)同温同压下,同体积的NH3和H2S的质量比是;同质量的NH3和H2S的体积比是;若两者所吉氢原于个数相等,NH3和H2S的物质的量比是。
(4)将标准状况下的NH3(g)VL溶于水中,得到密度为b g·cm-3的氨水a g,此时物质的量浓度为c mol·L-1,则溶于水中的NH3(g)的体积V是L(用a、b、c等表示)。
CoCl2·6H2O是一种饲料营养强化剂。以含钴废料(含少量Fe、Al等杂质)制取CoCl2·6H2O的一种新工艺流程如下图: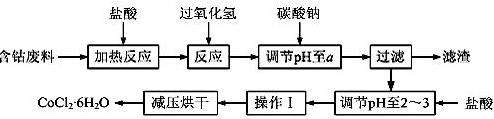
已知:
①钴与盐酸反应的化学方程式为:Co+2HCl=CoCl2+H2↑
②CoCl2·6H2O熔点86℃,易溶于水、乙醚等;常温下稳定无毒,加热至110~120℃时,失去结晶水变成有毒的无水氯化钴。
③部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
| 沉淀物 |
Fe(OH)3 |
Fe(OH)2 |
Co(OH)2 |
Al(OH)3 |
| 开始沉淀 |
2.3 |
7.5 |
7.6 |
3.4 |
| 完全沉淀 |
4.1 |
9.7 |
9.2 |
5.2 |
请回答下列问题:
(1)在上述新工艺中,用“盐酸”代替原工艺中“盐酸与硝酸的混酸”直接溶解含钴废料,其主要优点为 。
。
(2)加入碳酸钠调节pH至a,a的范围是;
(3)操作Ⅰ包含3个基本实验操作,它们是、和过滤。
(4)制得的CoCl2·6H2O需减压烘干的原因是 。
(5)为测定产品中CoCl2·6H2O含量,某同学将一定量的样品溶于水,再向其中加入足量的AgNO3溶液,过滤,并将沉淀烘干后称量其质量。通过计算发现产品中CoCl2·6H2O的质量分数大于100%,其原因可能是(任写1点)。
(12分)
随着氮氧化物污染的日趋严重,国家将于“十二五”期间加大对氮氧化物排放的控制力度。目前,用活性炭还原法处理氮氧化物是消除氮氧化物污染的有效方法。
⑴已知产物 A、B 都是参与大气循环的气体,请结合下表数据写出NO与活性炭反应的化学方程式:
⑵某研究小组向某密闭容器加入一定量的活性炭和NO,恒温(T1℃)条件下反应,反应进行到不同时间测得各物质的浓度如下:
浓度/mol·L-1
时间/min |
NO |
A |
B |
||
| 0 |
0. 10 |
0 |
0 |
||
| 10 |
0.058 |
0.021 |
0.021 |
||
| 20 |
0.040 |
0.030 |
0.030 |
||
| 30 |
0.040 |
0.030 |
0.030 |
||
| 40 |
0.032 |
0. 034 |
0.017 |
||
| 50 |
0.032 |
0. 034 |
0.017 |
①T1℃时,求该反应平衡常数(列出K的表达式,要求计算过程)。
②30min后,改变某一条件,反应重新达到平衡,则改变的条件可能是 。
③若30min后升高温度至T2℃,达到平衡时,容器中NO、A、B的浓度之比为5:3:3,则该反应的△H 0(填“>”、“=”或“<”)。
④压缩容器体积,增大压强对该反应的反应速率和平衡移动的影响是 。
I.冠心平F是降血脂、降胆固醇的药物,它的一条合成路线如下: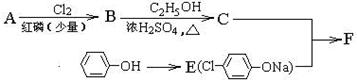
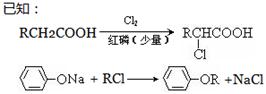 (注:R表示烃基或H原子)
(注:R表示烃基或H原子)
⑴ A为羧酸,其分子式为C4H8O2,8.8gA与足量NaHCO3溶液反应生成L CO2(标准状况,不考虑CO2溶于水)。
⑵写出符合A分子式羧酸类物质的结构简式: 。
⑶已知A→B属于取代反应,B为一卤代羧酸,其核磁共振氢谱只有两个峰,写出B→C的反应方程式:  。
。
⑷写出F的结构简式: 。
II.按如下路线,由C可合成酯类高聚物H: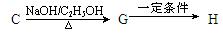
⑸写出G→H的反应方程式: 。
有以下几种物质:
| A.熔融状态的硝酸钾 | B.稀硫酸 | C.醋酸(CH3COOH) | D.BaSO4固体 |
E、酒精 F、干冰 G、铝 H、食盐水 I、石墨
在空格中填写正确的序号。
(1)以上物质中能导电的是 ;
(2)以上物质中属于电解质的是 ;
(3)以上物质中属于非电解质的是  。
。