某食盐样品中含有少量沙土、氯化钙和氯化镁。以下是除去食盐样品中沙土、氯化钙和氯化镁的实验流程:
根据流程图回答:
(1)操作Ⅰ的名称是 ,加入的试剂A是 ,沉淀是 ;
(2)写出NaOH与杂质反应的化学方程式: ;
(3)加入试剂B的目的是 ;
(4)蒸发结晶时用到玻璃棒的作用是 。
草酸钙(化学式为CaC2O4,相对分子质量为128)是一种难溶于水的白色固体,受热能分解。小红同学为了探究其在加热条件下发生的变化,进行如下实验:取12.8g草酸钙固体在不断加热的条件下测得剩余固体的质量随时间变化如右图所示。请回答下列问题: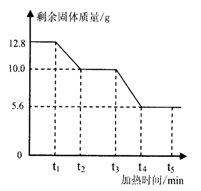
(1)t1~t2时间段内固体质量减少的原因是产生了一种极易与血红蛋白结合的有毒气体,该气体的化学式为 ;同时生成一种白色同体,它与大理石的主要成分相同,则该段时问内反应的化学方程式为
(2)t2~t3时间段内固体质量不变的原因是
(3)t3~t4时间段内反应的化学方程式为
根据初中所学的知识并结合下列仪器回答问题:
(1)写出下列仪器的名称:f
(2)实验室选取d、e、h、j四种仪器制取并收集氧气时,反应的化学方程式为
(3)小曼同学在实验室制取二氧化碳,除了选用了仪器b、g 外还需选择上述仪器中的 (填写字母)。检查完装置的气密性后,应先往仪器b中加入的药品是 ,反应的化学方程式是 。若收集的CO2通入澄清石灰水始终不见浑浊,原因是 。
(4)右图F装置可用来测量生成的CO2气体的体积,其中在水面上放一层植物油的目的是 。
(5)检验一瓶二氧化碳是否已经集满的方法是
(6)小淇同学用浓盐酸与大理石在上述装置中反应,制取CO2并检验其有关的性质,观察到烧杯中紫色石蕊溶液变红色,对可能造成这一现象的解释不合理的是 。(填序号)
A.产生的CO2直接使石蕊溶液变红;
B.产生的CO2与水反应生成碳酸,使石蕊溶液变红;
C.挥发出的氯化氢溶于水,使石蕊溶液变红。
在一定条件下,科学家利用从烟道气中分离出的CO2与太阳能电池电解水产生的H2合成甲醇(CH3OH)同时生成水,其过程如下图所示,试回答下列问题:
注:上述合成路线中用到15%~20%的乙醇胺(HOCH2CH2NH2),它的作用是CO2吸收剂。
(1)试写出上述合成线路中的两个化学反应的化学方程式:
①_________________________;
②_________________________。
(2)上述合成路线对于环境保护的价值在于____________________________。
(3)上述合成线路中可以循环利用的物质为_______________
混合气体可能有H2、CO2、CO中的一种或几种组成,为了验证其组成,现实验如下:(1)将该气体通入澄清石灰水,石灰水不变浑浊(2)将气体点燃,气体能燃烧,在火焰上方罩一只干而冷却的烧杯,烧杯内壁有水珠出现。则该气体一定有 ,可能有 ,一定没有 。
除杂
⑴要除去CO气体中混有的少量CO2,反应的化学方程式____________________
⑵要除去CO2气体中混有的少量CO,反应的化学方程式____________________