有机化合物是合成维生素类药物的中间体,其结构简式为:

的合成线路如下:

其中分别代表一种有机化合物,合成路线中的部分产物及反应条件已略去。
已知:

请回答下列问题:
(1)的分子式是
(2)第①步反应的化学方程式是
(3)的名称(系统命名)是
(4)第②~⑥步中属于取代反应的有
(5)第④步反应的化学方程式是
(6)写出同时满足下列条件的E的所有同分异构体的结构简式
①只含有一种官能团;②链状结构且无;③核磁共振氢谱只有2种峰。
(8分)现有HNO3和NaNO3的混合溶液200mL,其中 HNO3和NaNO3的物质的量浓度均为1 mol/L。若要使 HNO3和NaNO3的物质的量浓度分别为2 mol/L 和0.2 mol/L,应加入63%的浓硝酸(密度为1.2g/cm3)________mL,再加入蒸馏水稀释至_______mL才能实现。
(12分)实验室配制460mL0.100mol/LNa2CO3溶液回答下列问题,现有下列仪器
A 烧杯 B 100mL量筒 C 100mL容量瓶 D药匙E.玻璃棒 F.托盘天平
(1)配制时,必须使用的仪器有___________(填代号),还缺少的仪器是_______________。该试验中两次用到玻璃棒,其作用分别是___________________,_________________。
(2)应用托盘天平称取Na2CO3·10H2O晶体的质量为_________,若加蒸馏水不慎超过刻度线,处理的方法是______________。
(3)若实验遇下列情况,溶液的浓度偏高的是()
A溶解后没有冷却便进行定容
B摇匀后发现液面低于刻度线,滴加蒸馏水至刻度线再摇匀
C定容时俯视容量瓶的刻度线
D.容量瓶内壁附有水珠而未干燥处理
F.称取的Na2CO3·10H2O晶体失去了部分结晶水
(4)若取50.0mL上述已配好的溶液,与另一150mL0.200mol/L的Na2CO3溶液混合,最后得到的溶液的物质的量浓度为_________________(设溶液的体积变化可忽略)。
(12分)粗食盐常含有少量K+、Ca2+、Mg2+、Fe3+、SO 等杂质离子,实验室提纯NaCl的流程如下:
等杂质离子,实验室提纯NaCl的流程如下: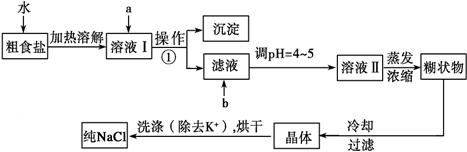
提供的试剂:饱和Na2CO3溶液、饱和K2CO3溶液、NaOH溶液、BaCl2溶液、Ba(NO3)2溶液、75%乙醇、四氯化碳、稀盐酸。
(1)欲除去溶液Ⅰ中的Ca2+、Mg2+、Fe3+、SO ,选出a所代表的试剂,按滴加顺序依次为____________________ (只填化学式)。
,选出a所代表的试剂,按滴加顺序依次为____________________ (只填化学式)。
(2)如何检验 SO 是否沉淀完全。
是否沉淀完全。
(3)调节pH 的目的,试剂b是(填名称)。
(4)洗涤除去NaCl晶体表面附带的少量KCl,选用的试剂为_________,使用该试剂的目的是。
(10分)某溶液中可能含有下列6种离子中的某几种:Cl-、SO 、NH4+、CO
、NH4+、CO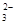 、K+、Na+。为确认溶液组成进行如下实验:(1)200mL上述溶液,加入足量BaCl2溶液,反应后将沉淀过滤、洗涤、干燥,得沉淀4.30g,向沉淀中加入过量的盐酸,有2.33g沉淀不溶。(2)向(1)的滤液中加入足量的NaOH溶液,加热,产生能促使湿润红色石蕊试纸变蓝的气体1.12L(已换算成标准状况,假定产生的气体全部逸出)。
、K+、Na+。为确认溶液组成进行如下实验:(1)200mL上述溶液,加入足量BaCl2溶液,反应后将沉淀过滤、洗涤、干燥,得沉淀4.30g,向沉淀中加入过量的盐酸,有2.33g沉淀不溶。(2)向(1)的滤液中加入足量的NaOH溶液,加热,产生能促使湿润红色石蕊试纸变蓝的气体1.12L(已换算成标准状况,假定产生的气体全部逸出)。
(1)溶液一定存在的离子有,可能存在的离子有。
(2)原溶液中c(CO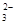 )为,c(NH4+)c(SO
)为,c(NH4+)c(SO ) (填“>、<或=”)。
) (填“>、<或=”)。
(3)如果上述6种离子都存在,则c(Cl-)c(SO ) (填“>、<或=”)。
) (填“>、<或=”)。
(14分)(1)O2、SO2、SO3三者质量之比为1∶2∶5,则它们的氧原子数之比为
(2)某金属氯化物MCl2 40.5 g中含有0.6 mol Cl-,则MCl2的摩尔质量为,金属M的相对原子质量为。
(3)在无土栽培中,配制1 L内含5 mol NH4Cl、1.6 mol KCl、2.4 mol K2SO4的某营养液,若用KCl、NH4Cl、(NH4)2SO4配制,则需这三种固体的物质的量分别为、、。
(4)相同浓度的NaCl、MgCl2、AlCl3溶液,分别与AgNO3溶液反应,当生成的AgCl沉淀的质量之比为3∶2∶1时,三种溶液的体积比为________。