下列各选项中两种粒子所含电子数不相等的是
| A.羟基(-OH)和氢氧根(OH-) |
| B.亚硝酸(HNO2)和亚硝酸根(NO2‑) |
| C.硝基(-NO2)和二氧化氮(NO2) |
| D.羟甲基(-CH2OH)和甲氧基(CH3O-) |
下列叙述不正确的是()
| A.电解法精炼铜时,纯铜作阴极,Cu2+发生还原反应 |
| B.电解饱和食盐水时,用铁作阳极,C1-发生氧化反应 |
| C.电镀锌时,金属锌作阳极,电镀液可用硫酸锌溶液 |
| D.铜锌原电池中,锌作负极,电子沿导线从锌极流向铜极 |
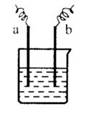
右图中,两电极上发生的电极反应如下:a极: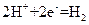 ↑,
↑, 
b极: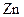 -2
-2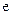 =
= 。则以下说法不正确的是()
。则以下说法不正确的是()
| A.该装置可能是电解池 |
| B.该装置中电解质溶液pH可能等于7 |
| C.a、b可能是同种电极材料 |
| D.该过程中能量的转换一定是化学能转化为电能 |
用NaOH溶液吸收二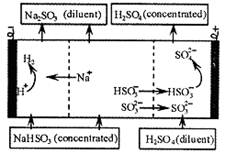
氧化硫,将所得的混合液进行电解循环再生,这种新工艺叫再生循环脱硫法。其中阴阳膜组合循环再生机理如图,则下列有关说法正确的是()
| A.阳极区酸性减弱 |
| B.阴极区电极反应式为:2H++2e—=H2↑ |
| C.该过程主要是为了获得H2SO4 |
| D.电解时两个电极都只能用惰性材料 |
如右图所示装置,两玻璃管中盛满滴有酚酞溶液的NaCl饱和溶液,C(Ⅰ)、C(Ⅱ)为多孔石墨电极。接通S1后,C(Ⅰ)附近溶液变红,两玻璃管中有气体生成。一段时间后(两玻璃管中液面未脱离电极),断开S1,接通S2,电流表的指针发生偏转,说明此时该装置形成了原电池,关于该原电池的叙述正确的是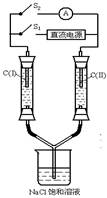
| A.C(I)的电极反应式是2H++2e- = H2↑ |
| B.C(II)的电极反应式是Cl2+2e-=2Cl- |
| C.C(I)的电极名称是阴极 |
| D.C(II)的电极名称是负极 |
电动自行车由于灵活、快捷、方便,已成为上班族的主要代步工具,其电源常用铅蓄电池,反应原理为:PbO2+Pb+2H2SO4 2PbSO4+2H2O下列叙述正确的是()
2PbSO4+2H2O下列叙述正确的是()
| A.放电时PbO2是电池的负极,电解质溶液的密度逐渐减小 |
| B.放电时负极的电极反应式为:Pb+SO42--2e-=PbSO4↓ |
| C.电池充电时,PbO2得电子被氧化 |
| D.电池充电时,阴极电极反应式为:PbSO4+2H2O-2e-=PbO2+SO42-+4H- |