硫酸是一种重要的化工产品,目前主要采用“接触法”进行生产。下列对于反应 2SO2+O2
2SO2+O2 2SO3的说法中正确的是:( )
2SO3的说法中正确的是:( )
| A.只要选择适宜的条件,SO2和O2就能全部转化为SO3 |
| B.该反应达到平衡后,反应就完全停止了,即正逆反应速率均为零 |
| C.在工业合成SO3时,要同时考虑反应速率和反应能达到的限度两方面的问题 |
| D.在达到平衡的体系中,充入由18O原子组成的O2后, 18O仅存在于SO2和SO3中 |
今有一混合物的水溶液,只可能含有以下离子中的若干种:Na+、NH 、Ba2+、Cl-、CO
、Ba2+、Cl-、CO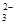 、SO
、SO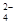 。现取两份200mL溶液进行如下实验:①第一份加足量NaOH溶液,加热,收集到气体1.36g;②第二份加足量BaCl2溶液后,得干燥沉淀12.54g,经足量盐酸洗涤、干燥后,沉淀质量为4.66g。根据上述实验,以下推测正确的是
。现取两份200mL溶液进行如下实验:①第一份加足量NaOH溶液,加热,收集到气体1.36g;②第二份加足量BaCl2溶液后,得干燥沉淀12.54g,经足量盐酸洗涤、干燥后,沉淀质量为4.66g。根据上述实验,以下推测正确的是
A.一定不存在Ba2+,NH 可能存在 可能存在 |
B.CO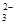 一定不存在 一定不存在 |
| C.Na+一定存在 | D.一定不存在Cl- |
设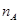 为阿伏加德罗常数的数值,下列说法正确的是
为阿伏加德罗常数的数值,下列说法正确的是
A.16g 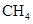 中含有4 中含有4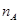 个C-H键 个C-H键 |
B.1mol·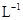  溶液含有 溶液含有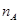 个 个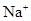 |
C.1mol Cu和足量稀硝酸反应产生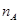 个NO分子 个NO分子 |
D.常温常压下,22.4L 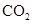 中含有 中含有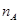 个 个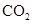 分子 分子 |
将钠和碳分别置于右图所示的两个盛满氧气的集气瓶中燃烧完毕后,打开装置中的两个活塞,这时观察到()
、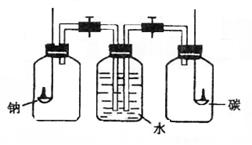
| A.水进入右瓶 | B.水进入左瓶 |
| C.水同时进入两瓶 | D.水不进入任何一瓶 |
某同学为证明NaOH溶液能使酚酞试液变红是OH-的性质,他所设计的下列实验中没有意义的是
| A.取KOH、Ba(OH)2、Ca(OH)2溶液分别与酚酞试液作用,观察溶液颜色 |
| B.取NaCl溶液与酚酞试液作用,观察溶液颜色 |
| C.测定NaOH的溶解度,证明其易溶于水,并观察溶液的颜色 |
| D.向滴有酚酞的NaOH溶液中加入盐酸,观察溶液的颜色 |
除去NaCl中含有的Ca2+、Mg2+、SO42-、HCO3-等离子,通常采用以下四种试剂:①Na2CO3②BaCl2③NaOH④HCl。加入试剂合理的操作顺序是()
| A.①②③④ | B.③①②④ | C.④②①③ | D.③②①④ |