如下图所示进行实验,同时将针筒内全部液体迅速注入容器中,实验内容如下表所示。

| 实验编号 | 容器I | 针筒I | 容器II | 针筒II | 红墨水液面位置 |
| 二氧化碳(充满) | 10 澄清石灰水 | 二氧化碳(充满) | 10 水 | 保持左高右低 | |
| 0.55 锌 | 15 盐酸 | 0.24 镁 | 15 盐酸 |
(1)实验开始前红墨水左右两端液面保持相平。容器I、II体积相同,装置气密性良好。
(2)实验
中,容器I内产生的现象是
(3)实验
中,针筒I、II内盐酸足量且溶质质量分数相同,产生气泡更剧烈的容器是
(4)红墨水的位置变化情况是
化学就在我们身边,它与我们的生活息息相关。请从A熟石灰;B纯碱;C.天然气;D.硝酸钾;E.纤维素;F.维生素;G.盐酸;H.硫酸这八种物质中,选择适当的字母序号填空。
(1)人体胃液中含有的酸是________。
(2)我国实施的“西气东输”工程输送的物质是________。
(3)侯氏联合制碱法中的“碱”是________。
(4)可作为农田施用的复合肥是________。
(5)棉、麻等天然植物纤维的主要成分是______。
(6)能于改良酸性土壤并可用于配置农药波尔多液的是________。
一种新型的甜味剂木糖醇在市场上大受欢迎。木糖醇的化学式为C5H12O5,它最大的优势是可以减少或者预防蛀牙。木糖醇的甜度与蔗糖相当,但热量只有蔗糖的60%。据介绍,木糖醇是一种原产于芬兰的天然甜味剂,后来日本从白桦树和玉米芯等植物中提炼出这种天然甜味剂。由于木糖醇不能被细菌分解,利用它来取代甜品中的糖分,可以防止蛀牙。而在口香糖里添加木糖醇是目前国际上最为普遍的防蛀方法。
(1)木糖醇是一种________________(填“有机化合物”或“无机化合物”),属于营养素中的________,相对分子质量为________。
(2)请你设计实验证明木糖醇中含有碳元素和氢元素。
| 操作 |
现象 |
结论 |
维生素C又名抗坏血酸,可溶于水,具有酸性,且在酸性环境中较稳定,在高温时易被破坏,主要存在于蔬菜和水果中,它能增强人体对疾病的抵抗能力。
(1)维生素C是我们必需的营养物质中的______________。
(2)下列物质中能与维生素C反应的是______________________________ (填序号)。
| A.食盐 | B.纯碱 | C.硫酸钾 | D.苛性钠 |
(3)你认为如何食用黄瓜才能充分利用黄瓜中的维生素C?____________________________。
邓小平同志故居果山村盛产枇杷,有“枇杷之乡”之美誉。下图是这种枇杷的部分营养成分,请据图回答: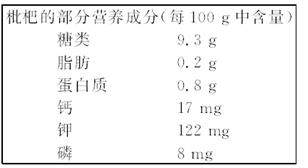
(1)图中的钙、钾、磷是指__________。
A.分子 B.原子 C.元素 D.单质
(2)图中出现了六大营养素中的________类,能提供能量的营养素有__________种。
(3)糖类、蛋白质、脂肪都属于__________(填“有机物”或“无机物”)。
(4)枇杷适宜生长在pH为6左右的土壤中。若某土壤的pH为3 ,经改良后可种植枇杷。下列物质,既可用来改良土壤酸性,又能给土壤施肥的物质是____________。
A.生石灰
B.熟石灰
C.过磷酸钙
D.草木灰(主要成分碳酸钾)
中考期间同学们很辛苦,要注意生活中的点滴才能保证中考顺利进行,取得好成绩。请你用所学知识回答下列问题。
(1)均衡膳食。下列食物中,能提供大量维生素的是________(填序号)。
A.蔬菜 B.牛奶 C.大米
(2)严禁吸烟。香烟烟气中含有几百种对人体有害的物质,毒性作用最大的有________、尼古丁和含有致癌物的焦油等。
(3)常开窗户呼吸新鲜空气。你能闻到窗外的花香是因为____________________。