X、Y、Z、U为原子序数依次增大的前四周期元素,X、Y、Z三种元素位于同一周期,其中基态Y原子的2p轨道处于半充满状态,Y和Z的单质可以通过分离液态空气的方法大量制得,且XZ2与Y2Z互为等电子体。含U的化合物的焰色为紫色。试回答下列问题:
(1)U单质的原子堆积方式为__________________,Y的价电子排布式为__________________。
(2)化合物甲由Z、U两元素组成,其晶胞如图所示。
①甲的化学式为____________。
②下列有关该晶体的说法中正确的是________(选填选项字母)。
A.每个晶胞中含有14个U+ 和13个Z2-
B.晶体中每个U+ 周围距离最近的U+ 有6个
C.该晶体属于离子晶体
③甲的密度为a g·cm-3,则晶胞的体积是_____________ m3(只要求列出计算式,阿伏加德罗常数的值用NA表示)。
能源是现代社会发展的三大支柱之一。化学在提高能源的利用率和开发新能源中起到了重要的作用。
(1)下列说法中,正确的是。(填序号)
| A.煤、石油和天然气都是可再生的能源 |
| B.目前使用的手机电池为二次电池,放电时是将化学能转化为电能 |
| C.人体运动所消耗的能量与化学反应无关 |
| D.人类目前所直接利用的能量大部分是由化学反应产生的 |
(2)电能是现代社会中应用最广泛的二次能源,下列装置中能够实现化学能转化为电能的是(填序号)。写出该装置正极反应的电极反应式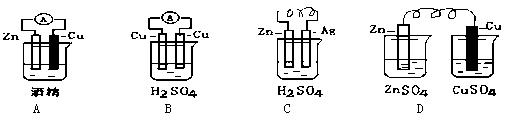
(3)锌锰干电池是目前使用最广泛的一种电池,其正极材料是石墨棒,它在放电时总反应式可表示为:Zn+ 2 MnO2 + 2 NH4+ ="=" Zn2+ + Mn2O3(S)+ 2NH3 + H2O。写出该电池负极反应的电极反应式。当电极锌消耗6.5g时,可对外提供的电子是mol。
(4)右图是氢氧燃料电池构造示意图(电解质溶液为稀硫酸)。关于该电池的说法不正确的是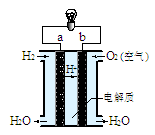
①.a极是负极
②.正极的电极反应是:O2+2H2O+4e-=4OH-
③.该装置可以将化学能完全转化为电能
④.氢氧燃料电池是环保电池
(5)人类在使用能源的过程中会产生环境问题。利用化学反应可以有效的进行治理。减少汽车等机动车尾气污染可在汽车尾气系统中增加催化转化装置,尾气中的CO、NO在催化剂的作用下反应生成两种参与大气循环的无毒气体,写出该反应的化学方程式。
下表为元素周期表的一部分,请参照元素①-⑨在表中的位置,用化学用语回答下列问题:
族 周期 周期 |
IA |
0 |
||||||
| 1 |
① |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
|
| 2 |
② |
③ |
④ |
|||||
| 3 |
⑤ |
⑥ |
⑦ |
⑧ |
⑨ |
 (1)9种元素中,原子半径最小的是。
(1)9种元素中,原子半径最小的是。
(2)④、⑤、⑥三种元素形成的简单离子中,离子半径最大的是。
(3)②、③、⑦的最高价含氧酸的酸性由强到弱的顺序是__________________。
(4)元素③的氢化物的电子式为;该氢化物常温下和⑨的氢化物两者反应的实验现象是,上述反应得到一种盐,属于化合物(填离子或共价)。检验该盐溶液中阳离子存在的方法是
(5)⑤和⑧两元素可形成化合物,该化合物灼烧时火焰颜色为色,用电子式表示该化合物的形成过程。
(6)写出⑥的最高价氧化物与⑤的最高价氧化物对应水化物反应的离子方程式。 (7)由表中两种元素的原子按1:1组成的常见液态化合物的稀溶液易被催化分解,可使用的催化剂为____________(填序号)。
(7)由表中两种元素的原子按1:1组成的常见液态化合物的稀溶液易被催化分解,可使用的催化剂为____________(填序号)。 A.MnO2 B.FeCl3 C.Na2SO3 D.KMnO4
A.MnO2 B.FeCl3 C.Na2SO3 D.KMnO4
工业上用乙烯和氯气为原料合成聚氯乙烯(PVC)。已知次氯酸能跟乙烯发生加成反应:CH2=CH2+HOCl→CH2(OH)CH2Cl。以乙烯为原料制取PVC等产品的转化关系如下图所示。
试回答下列问题:
(1)B中官能团是 G的结构简式是 。
(2)⑤、⑦的反应类型分别是: 、 。
(3)写出D的两种同分异构体的结构简式: 。
(4)写出反应⑥的化学方程式:______________________________________。
(5)写出C与D按物质的量之比为1∶2反应生成H的化学方程式:______ _。
在下列物质中选择相应的序号填空:
①甲烷②乙烯③甲苯④1-丁醇⑤乙酸乙酯⑥甘氨酸
Ⅰ.分子结构为正四面体的是;Ⅱ.能发生水解反应的是;
Ⅲ.能与溴水反应并使其褪色的是;Ⅳ.与酸或碱都能反应生成盐的是;
Ⅴ.能发生消去反应的是;
A~G是几种烃的分子球棍模型,据此回答下列问题: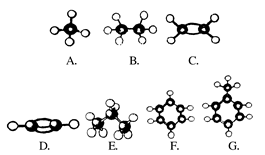
(1)常温下含碳量最高的气态烃是(填对应字母)________;
(2)能够发生加成反应的烃有(填数字)____种;
(3)一卤代物种类最多的是(填对应的字母)____;
(4)写出C发生加聚反应的化学方程式________________;
(5)写出G合成烈性炸药(TNT)的化学方程式____________。