某可逆反应从0—2分钟进行过程中, 在不同反应时间各物质的量的变化情况如下图所示。
(1)则该反应的化学方程式为 ;
(2)反应开始至2分钟时,能否用C表示反应速率? (填能或不能).若能,其反应速率为 _____ ;若不能,则其原因为 _________ ;
(3)2分钟后A、B、C各物质的量不再随时间的变化而变化,则此时v正(B)与v逆(C)的等量关系是 。
为防止在大灾之后疫病流行,全国各地向灾区运送了大量的各种消毒剂、漂白剂等。
(1) 过碳酸钠是一种有多用途的新型氧系固态漂白剂,化学式可表示为Na2CO3·3H2O2,它具有Na2C O3和H2O2的双重性质。过碳酸钠与下列物质均会发
O3和H2O2的双重性质。过碳酸钠与下列物质均会发 生化学反应而失效,其中过碳酸钠有发生了还原反应的是
生化学反应而失效,其中过碳酸钠有发生了还原反应的是
| A.MnO2 | B.KMnO4溶液 | C.Na2SO3溶液 | D.稀硫酸 |
(2) 漂白剂亚氯酸钠(NaClO2)在常温与黑暗处可保存一年,亚氯酸不稳定可分解,反应的离子方程式为HClO2→ClO2↑+H++Cl-+H2O(未配平)。当生成1molClO2时转移的电子数是
(3) 二氧化氯是目前国际上公认的第四代高效、无毒的广谱消毒剂,它可由KClO3在H2SO4存在下与SO2反应制得。请写出反应的离子方程式:
(4)有Fe2+、NO3-、Fe3+、NH4+、H+和H2O六种粒子,分别属于同一氧化还原反应中的反应物和生成物,则该反应中还原剂与氧化剂的物质的量之比为
(1)某化学反应可用下式表示:A + B ="=" C + D + H2O ,若A、D均可用于消毒,且C是家家户户的厨房必备的物质之一,
写出该反应的离子方程式:
(2)硝酸铅的稀溶液中,滴入几滴稀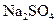 生成白色
生成白色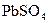 沉淀,再滴入数滴饱和NaAc溶液,微热,并不断搅动,沉淀慢慢溶解,以上发生的都是复分解反应,写出反应过程的离子方程式
沉淀,再滴入数滴饱和NaAc溶液,微热,并不断搅动,沉淀慢慢溶解,以上发生的都是复分解反应,写出反应过程的离子方程式
①②
(3)边微热边向铵明矾[NH4Al(SO4)2`12H2O]溶液中逐滴加入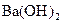 溶液至中性
溶液至中性
(提示:NH+ 4 、Al3+恰好完全反应)
①此时发生反应的离子方程式为
②向以上所得中性溶液中继续滴加稀硫酸,相关反应的离子方程式是:
硝酸与金属反应时,浓度越稀还原产物价态越低。现用一定量的铝粉与镁粉组成的混合物与100ml硝酸钾溶液与硫酸组成的混合溶液充分反应,反应过程中无任何气体放出,相反应后的溶液中逐滴加入4.00mol/L的NaOH溶液,加入的溶液体积与与产生的沉淀质量的关系如图所示。
回答下列问题:
(1)写出铝与混合溶液反应的离子方程式:
(2)参加反应硝酸根离子物质的量为mol
(3)参加反应的铝与镁的质量之比为
(4)混合液中硫酸的物质的量的浓度为mol/L
用电弧法合成的储氢纳米碳管常伴有大量的碳纳米颗粒(杂质),这种颗粒可用如下氧化法提纯。
(1)完成该反应的化学方程式:(系数按顺序填在答题卷上)
___ C+ ___ KMnO4+ ____ H2SO4→____CO2↑+ ____MnSO4 + ____K2SO4+ ____
(2)反应的氧化剂是,被还原的元素名称是;
(3)H2SO4在上述反应中表现出来的性质是(填选项编号)
| A.酸性 | B.氧化性 | C.吸水性 | D.脱水性 |
(4)上述反应中若产生2.24L(标准状况下)CO2气体,则转移的电子数是。
A、B、C、D都是中学化学中常见物质,其中A、B、C均含有同一种元素,在一定条件下相互转化关系如下(部分反应中的水已略去)。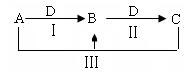
(1)若A为氯碱工业的产品,C为厨房中 的用品。
的用品。
①D的电子式是 。
。
②反应Ⅲ的离子方程式是。
③氯碱工业制备A的化学方程式是
 ,其中两种产物可与KI溶液反应制得一种化工原料,若消耗0.1 mol KI转移电子0.6 mol,则三种物质间反应的离子方程式是
,其中两种产物可与KI溶液反应制得一种化工原料,若消耗0.1 mol KI转移电子0.6 mol,则三种物质间反应的离子方程式是 。
。
(2)若A、D均为单质,且A为黄绿色气体 ,D元素的一种红棕色氧化物常用作颜料。
,D元素的一种红棕色氧化物常用作颜料。
①反应Ⅲ的离子方程式是。
②B可作净水剂,其原理是 (用离子方程式表示)。在使用时发现B不能使酸性废水中的悬浮物沉降除去,其原因是。
(用离子方程式表示)。在使用时发现B不能使酸性废水中的悬浮物沉降除去,其原因是。