下列大小关系比较正确的是
| A.离子半径:F-<Na+<Mg2+ |
| B.电负性:C<O<N |
| C.氢化物的沸点:NH3<PH3<AsH3 |
| D.碱性: NaOH)>Mg(OH)2> Al(OH)3 |
下列说法正确的是
| A.自发反应的熵一定增大,非自发反应的熵一定减小 |
| B.非自发反应在任何情况下都不会发生 |
C.常温下,反应C(s)+CO2(g) 2CO(g)不能自发进行,则该反应的ΔH>0 2CO(g)不能自发进行,则该反应的ΔH>0 |
| D.需要加热才能发生的反应一定是吸热反应 |
欲配制100mL 1.0 mol/L Na2CO3溶液,正确的方法是()
①将10.6 g Na2CO3 溶于100mL水中
②将28.6g Na2CO3·10H2O溶于少量水中,再用水稀释至100 mL
③将20 ml 5.0 mol/L Na2CO3溶液用水稀释至100 mL
| A.①② | B.②③ | C.只有② | D.①②③ |
V mLAl2(SO4)3溶液中含有Al3+a g,取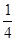 V mL溶液稀释到4V mL,则稀释后溶液中SO42-的物质的量浓度是()
V mL溶液稀释到4V mL,则稀释后溶液中SO42-的物质的量浓度是()
A.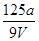 mol/L mol/L |
B. mol/L mol/L |
C.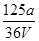 mol/L mol/L |
D.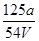 mol/L mol/L |
已知1.505×1023个X气体分子的质量为8g,则X气体的摩尔质量是
| A.16g | B.32g | C.64g /mol | D.32g /mol |
将30mL 0.5mol/LNaOH溶液加水稀释到500mL,稀释后溶液中NaOH的物质的量的浓度为
| A.0.03mol/L | B.0.04mol/L | C.0.05mol/L | D.0.3mol/L |