八角茴香是中国传统的香料和中药,八角茴香含有一种重要成分莽草酸,莽草酸是目前世界上被证明是对抗禽流感的唯一良方—“达菲”的原材料。莽草酸的结构简式为:下列关于莽草酸的说法正确的是
| A.该化合物的分子式为C7H11O5 |
| B.该化合物的分子处于同一平面的原子只有4个 |
| C.该化合物可以与溴水、NaOH、NaHCO3发生反应 |
D.该化合物在浓硫酸作用下加热不能制备得到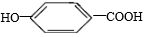 |
在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如右图所示,下列表述中正确的是()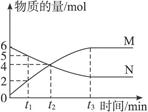
A.反应的化学方程式为2M N N |
B.t1时,正、逆反应速率相等,达平衡 |
| C.t3时,正反应速率大于逆反应速率 | D.t1时,N的浓度是M浓度的2倍 |
100 mL 6 mol·L-1的H2SO4跟过量的锌反应,在一定温度下,为减缓反应速率,但又不影响生成氢气的总量,可向反应物中加入适量的()
| A.硫酸钠固体 | B.水 |
| C.硫酸钾溶液 | D.硝酸钾溶液 |
下列哪些是影响化学反应速率的主要因素()
| A.压强 | B.温度 | C.催化剂 | D.反应物的性质 |
100 mL浓度为2 mol·L-1的盐酸跟过量的锌片反应,为加快反应速率,又不影响生成氢气的总量,可采用的方法是()
| A.加入适量6 mol·L-1的盐酸 | B.加入少量醋酸钠固体 |
| C.加热 | D.加入少量金属钠 |
盐酸和K2CO3反应时,能使反应的最初速率明显加快的是()
| A.将盐酸用量增加一倍 | B.盐酸的浓度增加一倍,用量减半 |
| C.温度升高30 ℃ | D.增加K2CO3粉末的量 |