下列反应既是氧化还原反应,又是吸热反应的是
| A.铝片与稀H2SO4反应 | B.Ba(OH)2·8H2O与NH4Cl的反应 |
| C.灼热的木炭与CO2反应 | D.甲烷在O2中的燃烧反应 |
25 ℃ 时,将某一元酸HA和NaOH溶液等体积混合(体积变化忽略不计),测得反应后溶液的pH如下表:
下列判断不正确的是
A、X>0.05
B、将实验①所得溶液加水稀释后,c(OHˉ )/c(A-)变大
C、实验①所得溶液c(A-)+c(HA)="0.10" mol·L-1
D、实验②所得溶液: c(Na+)+c(OH-)= c(A-)+c(H+)
下列根据实验操作和实验现象所得出的结论,正确的是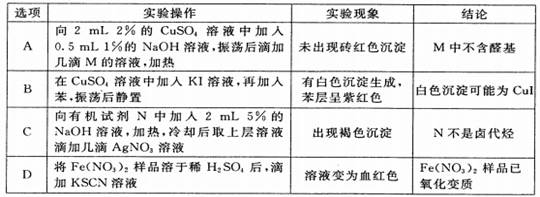
向某含有SO32-、SiO32-、CO32-、Br-、Na+的溶液中缓慢通入C12直至过量,下列对该反应过程的判断不正确的是
| A.整个过程共发生2个氧化还原反应 |
| B.所有阴离子的浓度都发生了变化 |
| C.溶液的颜色发生了变化 |
| D.反应过程中既有气体产生,也有沉淀产生 |
下图是部分短周期元素原子序数与最外层电子数之问的关系图,下列说法中正确的是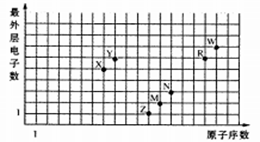
| A.元素对应的离子半径:Z>M>R>W |
| B.简单氢化物的沸点:W>R>Y>X |
| C.M、N、R、W的简单离子均能促进水的电离 |
| D.Z、X、R、W的最高价氧化物对应的水化物均能与N的单质反应 |
对于结构满足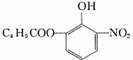 的有机物,下列描述中正确的是
的有机物,下列描述中正确的是
| A.分子中有2种含氧官能团 |
| B.能发生取代、加成、消去、氧化反应 |
| C.1 mol该有机物最多消耗3 mol NaOH |
| D.苯环上的一溴代物最多有3种 |