下列反应的离子方程式正确的是
| A.氯气与水反应:Cl2+H2O=2H++Cl-+ClO- |
| B.在稀氨水中通入过量CO2:NH3·H2O+CO2=NH4++HCO3- |
| C.用氯化铁溶液腐蚀电路板:Fe3++Cu=Fe2++Cu2+ |
| D.少量SO2通入Ca(ClO)2溶液中:SO2+H2O+Ca2++2ClO-=CaSO3↓+2HClO |
将4 mol A气体和2 mol B 气体在2 L的容器中混合并在一定条件下发生如下反应:2A(g)+B(g)  2C(g)若经2 s 后测得C的浓度为0.6 mol/L,下列几种说法正确的是:①用物质A表示的反应的平均速率为0.3 mol/(L·s);②用物质B表示的反应的平均速率为0.6 mol/(L·s);③反应达到平衡时,A、B、C的反应速率一定相等;④反应达到平衡时,A、B、C的物质的量均不再变化
2C(g)若经2 s 后测得C的浓度为0.6 mol/L,下列几种说法正确的是:①用物质A表示的反应的平均速率为0.3 mol/(L·s);②用物质B表示的反应的平均速率为0.6 mol/(L·s);③反应达到平衡时,A、B、C的反应速率一定相等;④反应达到平衡时,A、B、C的物质的量均不再变化
A.①③ B.①④ C.②③ D.③④
下列有关实验原理、方法和结论都正确的是
| A.加入氢氧化钠溶液并加热,产生的气体能使湿润红色石蕊试纸变蓝,一定有NH4+ |
| B.取少量X溶液,加入适量新制氯水,再加几滴KSCN溶液,溶液变红,说明X溶液中一定含有Fe2+ |
| C.向某溶液中滴加BaCl2溶液,若有白色沉淀,再滴加足量稀HNO3,若沉淀不溶解,则说明原溶液中一定含SO42- |
| D.某无色溶液用洁净铂丝蘸取溶液进行焰色反应,火焰呈黄色,则原溶液含有Na+无K+ |
下列离子方程式中,正确的
| A.在AlCl3溶液中加入过量氨水:Al3+ + 3NH3·H2O =Al(OH)3↓ + 3NH4+ |
| B.大理石加入过量盐酸中:CO32-+2H+= CO2↑+H2O |
| C.稀硫酸和Ba(OH)2溶液反应:Ba2++OH-+H++SO42-=BaSO4↓+H2O |
| D.在CuSO4溶液中加入Ba(OH)2溶液:Ba2+ + SO42- =BaSO4↓ |
用NA表示阿伏加德罗常数的值,下列说法正确的是
| A.标准状况下,5.6 L一氧化氮和5.6 L氧气混合后的分子总数为0.5NA |
| B.1 mol乙烷分子含有8NA个共价键 |
| C.58.5 g的氯化钠固体中含有NA个氯化钠分子 |
| D.在0.1 mol过氧化钠固体中,阴离子总数等于0.1 NA |
氧化还原反应与四种基本类型反应的关系如下图所示,则下列化学反应属于区域3的是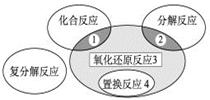
A.2H2+O2 2H2O 2H2O |
B.2NaHCO3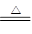 Na2CO3+H2O +CO2↑ Na2CO3+H2O +CO2↑ |
| C.Zn +H2SO4= ZnSO4 + H2↑ |
D.CuO+CO 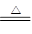 Cu + CO2 Cu + CO2 |