金属铜广泛地应用于电气、机械制造、国防等领域。
(1)Cu是元素周期表中第29号元素,写出第三周期基态原子未成对电子数与Cu相同且电负性最大的元素是 (填元素名称)。
(2)CuO受热易分解为Cu2O和O2,请从铜的原子结构来说明CuO受热易分解的原因:
。
(3)下图是铜的某种氧化物的晶胞示意图。已知该晶胞的边长为a cm,阿伏加德罗常数为NA,该晶体的密度为 。
(4)向硫酸铜溶液中滴加氨水会生成蓝色沉淀,在滴加氨水到沉淀刚好全部溶解可得到深蓝色溶液,继续向其中加入极性较小的乙醇可以生成深蓝色的[Cu(NH3)4]SO4·H2O沉淀。
①SO42-中S原子的杂化方式为 。
②NH3分子内的H—N—H键角 (填“大于”“等于”或“小于”)H2O分子内的H—O—H键角。
③S、N、O三种元素第一电离能由大到小的顺序为 。
2010年春,发生在滇、黔、桂、渝、川等省的严重旱情牵动了全国人民的心。水是组成生命体的重要化学物质,有关水的反应有很多。
(1)用电子式表示H2O的形成过程。
(2) H2O以键结合(填极性键、非极性键、离子键)
(3)在pH=1的溶液中,①NH4+、Al3+、Br-、SO42-② Na+、Fe2+、Cl-、NO3-
③K+、Ba2+、Cl-、NO3-④K+、Na+、HCO3-、SO42-四组离子中,一定大量共存的是(填序号)。
(4)在下列反应中,水仅做氧化剂的是(填字母,下同),水既不做氧化剂又不做还原剂的是。
| A.Cl2+H2O=HCl+HClO | B.2Na2O2+2H2O=4NaOH+O2↑ |
| C.CaH2+2H2O=Ca(OH)2+2H2↑ | D.3Fe+4H2O Fe3O4+4H2 Fe3O4+4H2 |
(5)已知KH和H2O反应生成H2和KOH,反应中1mol KH(填失去,得到)mol电子
(6)“神舟七号”飞船上的能量主要来自于太阳能和燃料电池,H2、O2和KOH的水溶液可形成氢氧燃料电池,负极的电极反应为,电极反应产生的水经冷凝后可作为航天员的饮用水,当得到1.8 L饮用水时,电池内转移的电子数约为。
下表是元素周期表的一部分,根据表中10种元素,用元素符号或化学式填空。
| 主族 周期 |
ⅠA |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
0族 |
| 2 |
① |
② |
||||||
| 3 |
③ |
④ |
⑤ |
⑥ |
⑦ |
|||
| 4 |
⑨ |
⑧ |
⑩ |
(1)①~⑩元素中,金属性最强的是;化学性质最不活泼的是。
(2)①~⑩元素中,最高价氧化物水化物呈两性的是,该化合物与NaOH溶液反应的离子方程式为;
(3)①~⑩元素中,最高价氧化物水化物酸性最强的是,碱性最强的是;
(4)⑤、⑥、⑧、⑨所形成的离子,其半径由小到大的顺序是;
用50mL 0.50 mol•L-1盐酸与50mL 0.55 mol•L-1 NaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。回答下列问题: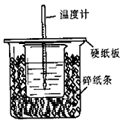
(1)从实验装置上看,图中尚缺少的一种玻璃用品是。
(2)烧杯间填满碎纸条的作用是。
(3)大烧杯上如不盖硬纸板,求得的中和热△H绝对值。(填偏大、偏小、无影响)
A、B、C、D、E五种短周期元素,它们的原子序数依次增大。A是元素周期表中原子半径最小的元素,B元素原子L层上的电子数为K层电子数的2倍;元素D的2价阴离子的核外电子排布与氖原子相同;E与A同主族;A和E这两种元素与D都能形成X2Y、X2Y2型化合物。请回答:
(1)写出元素的符号:A;B;C 。
(2)画出D的原子结构示意图_____;B在周期表的位置为第周期族。
(3)化合物A2D的电子式是_______________。
(4)B、C、D的气态氢化物稳定性由强到弱的顺序是_____________。(用化学式表示)
(5)B的最高价氧化物的结构式。
(6)写出单质E与A2D反应的离子方程式。
下图为周期表的一小部分,A、B、C、D、E、F的位置关系如图所示。其中B元素的最高价是负价绝对值的3倍,它的最高价氧化物中含氧60%,回答下列问题:
| F |
A |
|||
| D |
B |
E |
||
| C |
||||
(1)A在周期表中的位置为;E的离子结构示意图为;化合物DE3的电子式_______。
(2)F元素氢化物的空间构型为_______。
(3)D、B、E元素的最高价氧化物对应水化物的酸(或碱)性强弱顺序。(用化学式表示)
(4)B、C、E的气态氢化物稳定性由强到弱的顺序是________。(用化学式表示)
(5)B的单质与其最高价氧化物的水化物的浓溶液共热能发生反应,化学方程式为
。
(6)F2H4和FO2是一种双组分火箭推进剂。两种物质混合发生反应生成F2和H2O(g),已知8g F2H4气体在上述反应中放出142kJ热量,其热化学方程式为。
(7)请在答题卷相应位置画出金属与非金属元素的分界线。