下列反应的离子方程式正确的是
A.将氯气溶于水制备次氯酸:Cl2+H2O 2H++Cl-+ClO- 2H++Cl-+ClO- |
| B.少量CO2通入苯酚钠溶液中:2C6H5O-+CO2+H2O=2C6H5OH+CO32- |
| C.Na2O2与H2O混合:2Na2O2+2H2O=4Na++4OH-+O2↑ |
D.向NH4HCO3溶液中加过量的NaOH溶液并加热:NH4++OH- NH3↑+H2O NH3↑+H2O |
T℃时,向2.0 L恒容密闭容器中充入1.0 mol COCl2,反应COCl2(g) Cl2(g) + CO(g),经过一段时间后达到平衡。反应过程中测定的部分数据见下表:
Cl2(g) + CO(g),经过一段时间后达到平衡。反应过程中测定的部分数据见下表:
| t / s |
0 |
2 |
4 |
6 |
8 |
| n(Cl2) / mol |
0 |
0.16 |
0.19 |
0. 20 |
0.20 |
下列说法正确的是
A.反应在前2 s 的平均速率v(CO) =" 0.080" mol·L-1·s-1
B.保持其他条件不变,升高温度,平衡时c(Cl2) =" 0.11" mol·L-1,则反应的ΔH < 0
C.T℃时起始向容器中充入0.9 mol COCl2、0.20 mol Cl2和0.20 mol CO,达平衡前v正 > v逆
D.恒温恒容下,平衡后向体系内加入少量惰性气体,氯气的浓度不变
下列装置或操作能达到目的的是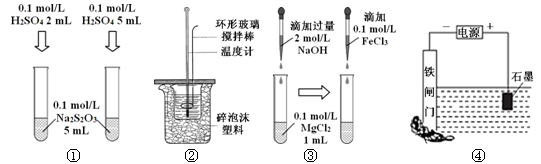
| A.装置①探究H2SO4浓度对反应速率的影响 |
| B.装置②可用于测定中和热 |
| C.装置③探究Mg(OH)2能否转化成Fe(OH)3 |
| D.装置④可保护铁闸门不被腐蚀 |
下列各溶液中,微粒的物质的量浓度关系正确的是
| A.0.1 mol/L Na2CO3溶液:c(OH-) = c(HCO3-) + c(H+) + 2c(H2CO3) |
| B.0.1 mol/L NH4Cl溶液:c(NH4+) = c(Cl-) |
| C.向醋酸钠溶液中加适量醋酸,得到的酸性混合溶液:c(Na+) > c(CH3COO-) > c(H+) > c(OH-) |
| D.向硝酸钠溶液中滴加稀盐酸得到pH = 5的混合溶液:c(Na+) = c(NO3-) |
下列叙述正确的是
| A.KSp[MgF2]>KSp[Mg(OH)2],不能实现Mg(OH)2转化为MgF2。 |
| B.常温下,同浓度的Na2S与NaHS溶液相比,Na2S溶液的pH大 |
| C.等物质的量浓度的NH4Cl溶液和NH4HSO4溶液,后者的c(NH4+)大 |
| D.FeCl3与KSCN反应达到平衡时,加入KCl溶液,则溶液颜色变深 |
某同学组装了如图所示的电化学装置,电极Ⅰ为 Zn,电极Ⅱ为Cu,其他电极均为石墨,则下列说法正确的是
|
A.电流方向:电极Ⅳ →○→电极Ⅰ
B.盐桥中的K+会移向ZnSO4溶液