近年来,加“碘”食盐较多的使用了碘酸钾(KIO3),碘酸钾在工业上可用电解法制取。以石墨和不锈钢为电极,以KI溶液为电解液,在一定条件下电解,反应的化学方程式为:KI+3H2O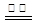 KIO3+3H2↑。下列有关说法不正确的是
KIO3+3H2↑。下列有关说法不正确的是
| A.电解时,石墨作阳极,不锈钢作阴极 |
| B.电解时的阳极电极反应式:I-−6e-+3H2O = IO3-+6H+ |
| C.当电解过程中转移3 mol e-时,理论上可制得KIO3 107 g |
| D.电解一段时间后,电解质溶液的pH变小 |
在反应H2 + Cl2= 2HCl中,已知断开1 mol H-H需要吸收436 kJ的能量,断开
1 mol Cl-Cl需要吸收243 kJ的能量,断开1 mol H-Cl需要吸收431 kJ的能量,判断该反应是
kJ的能量,断开1 mol H-Cl需要吸收431 kJ的能量,判断该反应是
| A.吸热反应 | B.放热反应 |
| C.放出862 kJ热量 | D.放出183 kJ热量 |
下列电子式正确的是
把a、b、c、d四块金属片浸入稀硫酸中,用导线两两相连组成原电池。若a、b相连时,a为负极;c、d相连时,电流由d到c;a、c相连时,c极上产生大量气泡,b、d相连时,b上有大量气泡产生,则四种金属的活动性顺序由强到弱的为
| A.a > c > d > b | B.a > b > c > d |
| C.c > a > b > d | D.b > d > c > a |
在图所示的装置中,a的金属性比氢要强,b为碳棒,关于此装置的各种叙述不正确的是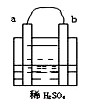
| A.碳棒上有气体放出,溶液的酸性减弱 |
| B.导线中有电子流动,电子从a极流到b极 |
| C.a是正极,b是负极 |
| D.a极上的电析反应式为:Zn-2e-=Zn2+ |
下列化学方程式中,Q1、Q2、Q3表示反应所放出的热量:
① 2H2 (g) + O2 (g) = 2H2O (g) + Q1 kJ; ② 2 H2 (g) + O2 (g) =" 2" H2O (l) + Q2 kJ;
③ H2 (g) + 1/2 O2 (g) = H2O (g) + Q3 kJ;
其中Q1、Q2、Q3的大小关系为
| A.Q1 = Q2 = Q3 | B.2Q3 = Q1 < Q2 | C.Q3 < Q2 < Q1 | D.Q1 < Q2 < 3Q3 |