在无色的水溶液中能大量共存的一组是( )
| A.Ba2+、AlO2-、OH-、Al3+ |
| B.K+、Fe3+、MnO4-、SCN- |
| C.Mg2+、H+、SO42-、S2O32- |
| D.NH4+、Ca2+、NO3-、Cl- |
下列说法中,正确的是
| A.22.4 L N2含阿伏加德罗常数个氮分子 |
| B.在标准状况下,22.4 L水的质量约为18g |
| C.22 g二氧化碳与标准状况下11.2 L HCl含有相同的分子数 |
| D.标准状况下,相同体积的任何气体单质所含的原子数相同 |
相同物质的量的不同固体或液体的体积并不相同,其主要原因是
| A.粒子大小不同 | B.粒子质量不同 |
| C.粒子间距离不同 | D.粒子间作用力不同 |
下列叙述中正确的是
| A.1molH2SO4的质量为98g·mol-1 | B.H2SO4的摩尔质量为98g |
| C.98gH2SO4含有NA个H2SO4分子 | D.6.02×1023个H2SO4分子的质量为9.8g |
下列实验操作不能用于物质分离的是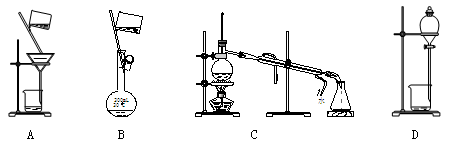
下列实验方案设计中,可行的是
| A.加稀盐酸后过滤,除去混在铜粉中的少量镁粉和铝粉 |
| B.用萃取的方法分离汽油和煤油 |
| C.用溶解、过滤的方法分离硝酸钾和氯化钠固体的混合物 |
| D.将氢气和氧气的混合气体通过灼热的氧化铜,以除去其中的氢气 |