“温室效应”是全球关注的环境问题之一。CO2是目前大气中含量最高的一种温室气体。因此,控制和治理CO2是解决温室效应的有效途径。
(1)将不同量的CO(g)和H2O(g)分别通入到体积为2L的恒容密闭容器中,进行反应CO(g)+H2O(g) CO2(g)+H2(g),得到如下三组数据:
CO2(g)+H2(g),得到如下三组数据:
| 实验组 |
温度/℃ |
起始量/mol |
平衡量/mol |
达到平衡所需时间/min |
||
| CO |
H2O |
H2 |
CO |
|||
| 1 |
650 |
4 |
2 |
1.6 |
2.4 |
6 |
| 2 |
900 |
2 |
1 |
0.4 |
1.6 |
3 |
| 3 |
900 |
a |
b |
c |
d |
t |
① 实验1条件下平衡常数K= (保留小数点后二位数字)。
② 实验3中,若平衡时,CO的转化率大于水蒸气,则a/b 的值 (填具体值或取值范围)。
③ 实验4,若900℃时,在此容器中加入10molCO、5molH2O、2molCO2、5molH2,则此时v(正) v(逆)(填“<”、“>”、“=”)。
(2)CO2在自然界循环时可与CaCO3反应,CaCO3是一种难溶物质,其Ksp=2.8×10—9。CaCl2溶液与Na2CO3溶液混合可形成CaCO3沉淀,现将等体积的CaCl2溶液与Na2CO3溶液混合,若Na2CO3溶液的浓度为2×10—4mo1/L,则生成沉淀所需CaCl2溶液的最小浓度为 。
(3)已知BaSO4(s) + 4C(s) ="4CO(g)" + BaS(s) △H1 =+571.2kJ/mol,
BaSO4(s) + 2C(s) = 2CO2(g) + BaS(s) △H2="+226.2" kJ/mol。
则反应C(s) + CO2(g) = 2CO(g)的△H3= kJ/mol。 (4)寻找新能源是解决温室效应的一条重要思路。磷酸亚铁锂LiFePO4是一种新型汽车锂离子电池,总反应为:FePO4+Li LiFePO4,电池中的固体电解质可传导Li+,则该电池放电时的正极和负极反应式分别为: 和 。若用该电池电解蒸馏水(电解池电极均为惰性电极),当电解池两极共有3360mL气体(标准状况)产生时,该电池消耗锂的质量为 。(Li的相对原子质量约为7.0)
(4)寻找新能源是解决温室效应的一条重要思路。磷酸亚铁锂LiFePO4是一种新型汽车锂离子电池,总反应为:FePO4+Li LiFePO4,电池中的固体电解质可传导Li+,则该电池放电时的正极和负极反应式分别为: 和 。若用该电池电解蒸馏水(电解池电极均为惰性电极),当电解池两极共有3360mL气体(标准状况)产生时,该电池消耗锂的质量为 。(Li的相对原子质量约为7.0)
油画置于空气中,天长日久就会生成黑色的PbS从而使油画的色彩变暗,若用H2O2来“清洗”,则可使PbS转变为白色的PbSO4,从而使油画“复原”。
(1)请写出“清洗”反应的化学方程式,此反应体现了H2O2的什么性质?
(2)若有0.100 mol的PbS参与反应,则在此反应中发生转移的电子的物质的量为_________mol。
用CO还原SO2(500℃,铝钒土作催化剂)是冶金工业中从烟道废气中回收硫的方法。
(1)写出有关反应的方程式:。
(2)某工厂每天排放500m3烟道废气,已知其中含SO2的体积分数为2.6%(已折算成标准状况),试计算用上述方法理论上可回收多少千克硫?
难溶化合物的饱和溶液存在溶解平衡,例如:AgCl(s) Ag++Cl-,Ag2CrO4(s)
Ag++Cl-,Ag2CrO4(s) 2Ag++
2Ag++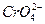 。在一定温度下,已知:Ksp(AgCl)=c(Ag+)·c(Cl-)=1.8×10-10,Ksp(Ag2CrO4)=[c(Ag+)]2·c(
。在一定温度下,已知:Ksp(AgCl)=c(Ag+)·c(Cl-)=1.8×10-10,Ksp(Ag2CrO4)=[c(Ag+)]2·c(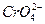 )=1.9×10-12,现用0.01 mol·L-1 AgNO3溶液滴定0.01 mol·L-1 KCl和0.001 mol·L-1 K2CrO4混合溶液,通过计算回答:
)=1.9×10-12,现用0.01 mol·L-1 AgNO3溶液滴定0.01 mol·L-1 KCl和0.001 mol·L-1 K2CrO4混合溶液,通过计算回答:
(1)Cl-、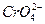 谁先沉淀?
谁先沉淀?
(2)当刚出现Ag2CrO4沉淀时,溶液中Cl-的物质的量浓度是多少?(设混合溶液在反应中体积不变)
汽油不完全燃烧的化学方程式为:
2C8H18(l)+23O2(g)====12CO2(g)+4CO(g)+18H2O(l)
人体吸进CO后,CO与人体血红蛋白结合而引起中毒。如果每辆汽车满负荷行驶,每天约有28.5g汽油不完全燃烧。现有200万人口的中等城市,如达到中等发达国家水平,平均每10人拥有1辆汽车。请计算这些汽车满负荷行驶时,每天可产生多少千克CO?
有Fe和Fe2O3混合物溶于500 mL稀HNO3中,放出2.24 L NO(标准状况),并剩余5.44 g Fe。向反应后的溶液中通入2.016 L Cl2(标准状况),恰好能使溶液中Fe2+全部氧化。求:
(1)稀HNO3物质的量浓度。
(2)混合物中的Fe的质量分数。