下列说法正确的是
| A. 14C与12C互为同素异形体 |
| B.高铁车厢大部分材料采用铝合金,因铝合金强度大、质量轻、抗腐蚀能力强 |
| C.NOx、CO2、PM2.5颗粒都会导致酸雨 |
| D.避免船体遭受腐蚀,在船舶的外壳装上若干锌块,称为外加电流的阴极保护法 |
常温下,下列各组离子在指定溶液中能大量共存的是()
| A.pH=1的溶液中:Fe2+、NO3-、SO42-、Na+ |
| B.水电离出的c(H+)=10-12 mol/L的溶液中:Ca2+、K+、Cl-、HCO3- |
| C.c(H+)/c(OH-)=1012的水溶液中:NH4+、Al3+、NO3-、Cl- |
| D.c(Fe3+)=0.1 mol/L的溶液中:K+、ClO-、SO42-、SCN- |
下列叙述正确的是()
| A.无论是纯水,还是酸性、碱性或中性稀溶液,在常温下,其c(H+)·c(OH-)=1×10-14 |
| B.c(H+)等于1×10-7 mol/L的溶液一定是中性溶液 |
| C.0.2 mol/L CH3COOH溶液中的c(H+)是0.1 mol/L CH3COOH溶液中的c(H+)的2倍 |
| D.任何浓度的溶液都可以用pH来表示其酸碱性的强弱。 |
在0.1 mol·L-1CH3COOH溶液中存在如下电离平衡:CH3COOH CH3COO-+H+,对于该平衡下列叙述正确的是()
CH3COO-+H+,对于该平衡下列叙述正确的是()
| A.加入水时,平衡逆向移动 |
| B.加入少量NaOH固体,平衡正向移动 |
| C.加入少量0.1 mol·L-1盐酸,溶液中c(H+)减小 |
| D.加入少量CH3COONa固体,平衡正向移动 |
室温下,用0.100 mol/L NaOH 溶液分别滴定20.00 mL 0.100 mol/L的盐酸和醋酸,滴定曲线如下图所示。下列说法正确的是()
| A.Ⅰ、Ⅱ分别表示盐酸和醋酸的滴定曲线 |
B.V(NaOH)=10.00 mL 时,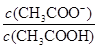 >1 >1 |
| C.pH=7时,两种酸所用NaOH溶液的体积相等 |
| D.V(NaOH)=20 .00 mL 时,c(Cl-)<c(CH3COO-) |
部分弱酸的电离平衡常数如下表:
| 弱酸 |
HCOOH |
HCN |
H2CO3 |
| 电离平衡常数(25℃) |
Ki=1.77×10-4 |
Ki=4.9×10-10 |
Ki1=4.3×10-7 Ki2=5.6×10-11 |
下列选项错误的是()
①2CN-+H2O+CO2=2HCN+CO32-
②2HCOOH+CO32-=2HCOO-+H2O+CO2↑
③中和等体积、等pH的HCOOH和HCN,消耗NaOH的量前者小于后者
④等体积、等浓度的HCOONa和NaCN溶液中所含离子总数前者小于后者
A.①② B.②③ C.③④ D.①④