下列实验操作、现象与结论对应关系正确的是
| 选项 |
实验操作 |
实验现象与结论 |
| A |
向盛有Fe(NO3)2溶液的试管中加入0.1mol·L-1 H2SO4溶液 |
试管口出现红棕色气体。则溶液中NO3-被Fe2+还原为NO2 |
| B |
向样品溶液中先滴加过量的稀盐酸,再滴加BaCl2溶液 |
先滴加稀盐酸无现象,滴加BaCl2后出现白色沉淀。说明样品溶液中一定含有SO42- |
| C |
向0.1mol·L-1 Na2CO3溶液中,滴加2滴酚酞显浅红色,微热 |
红色加深。说明盐类水解是吸热反应 |
| D |
向淀粉溶液中加入稀H2SO4,加热几分钟,冷却后再加入新制Cu(OH)2悬浊液,加热 |
无砖红色沉淀生成。表明淀粉没有水解生成葡萄糖 |
根据水溶液中存在的平衡关系,判断下列说法正确的是
| A.往水中滴加少量氢氧化钠稀溶液,Kw变小 |
| B.往AgCl悬浊液中加入0.1mol·L-1NaI溶液,无明显现象产生 |
| C.室温下,稀释0.1mol·L-1的醋酸,溶液中c(CH3COO-)·c(H+)不变 |
| D.等体积等浓度的氨水与盐酸混合后所得溶液显酸性 |
下列用来表示可逆反应2X(g)+Y(g) 3Z(g)△H<0的图像正确的是
3Z(g)△H<0的图像正确的是
以NA代表阿伏加德罗常数的值,下列说法申正确的是
| A.9g18O2含有的中子数为5NA |
| B.标准状况下,0.5NABr2所占的体积约为11.2L |
| C.常温下,1L0.1mol·L-1NH4NO3溶液中含有的NH4+数为0.1NA |
| D.一定条件下,lmol N2和3mol H2在密闭容器充分反应,生成N-H键的数目为6NA |
汽车剧烈碰撞时,安全气囊中发生反应:10NaN3+2KNO3=K2O+5Na2O+16N2↑。则列判断正确的是
| A.反应中KNO3为还原剂 |
| B.NaN3中氮元素为-3价 |
| C.标准状况下,若有6.5gNaN3参加反应,则生成3.584L N2 |
| D.若1mol KNO,参加反应,转移电子的物质的量为10mol |
下列针对甲、乙、丙、丁四种实验及装置的说法,不合理的是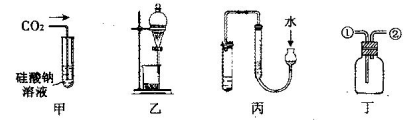
| A.甲可用来证明碳的非金属性比硅强 |
| B.乙装置可用于碘水中碘的萃取及分液 |
| C.用丙图示的方法检查此装置的气密性 |
| D.丁装置:从①进气可收集NO;从②进气可收集NH3 |