Ba(NO3)2可用于生产绿色烟花、绿色信号弹、炸药、陶瓷釉药等。钡盐行业生产中排出大量的钡泥[主要含有BaCO3、 BaSO3、 Ba( FeO2)2等],某主要生产BaCO3、 BaSO4的化工厂利用钡泥制取Ba(NO3)2晶体(不含结晶水),其部分工艺流程如下:
又已知:
①Fe3+和Fe2+以氢氧化物形式沉淀完全时,溶液的pH分别为3.2和9.7;
②Ba(NO3)2晶体的分解温度:592℃;
③KSP(BaSO4)=1.lxl0-10, KSP(BaCO3)=5.1×10-9.
(1)该厂生产的BaCO3因含有少量BaSO4而不纯,提纯的方法是:将产品加入足量的饱和Na2CO3溶液中,充分搅拌,过滤,洗涤。试用离子方程式说明提纯原理:______________ 。
(2)上述流程酸溶时,Ba(FeO2)2与HNO3反应生成两种硝酸盐,反应的化学方程式为:
。
(3)该厂结合本厂实际,选用的X为 (填序号);
| A.BaCl2 | B.BaCO3 | C.Ba(NO3)2 | D.Ba(OH)2 |
(4)中和I使溶液的pH为4~5目的是 ;
结合离子方程式简述原理 。
(5)从Ba(NO3)2溶液中获得其晶体的操作方法是 。
(6)测定所得Ba(NO3)2晶体的纯度:准确称取w克晶体溶于蒸馏水,加入足量的硫酸,充分反应后,过滤、洗涤、干燥,称量其质量为m克,则该晶体的纯度为 。
(I)某化学家根据“原子经济”的思想,设计了如下制备H2的反应步骤:
①CaBr2+H2O CaO+2HBr②2HBr+Hg
CaO+2HBr②2HBr+Hg HgBr2+H2
HgBr2+H2
③HgBr2+_____ _____ + ④2HgO
_____ + ④2HgO 2Hg+O2↑
2Hg+O2↑
请你根据“原子经济”的思想完成上述步骤③的化学方程式:_________。
根据“绿色化学”的思想评估该方法制H2的主要缺点:__________。
(II)氢气常用生产水煤气的方法制得。CO(g)+H2O(g) CO2(g)+H2(g)△H<0
CO2(g)+H2(g)△H<0
在850℃时,K=1。
(1)若升高温度到950℃时,达到平衡时K______1(填“大于”、“小于”或“等于”)
(2)850℃时,若向一容积可变的密闭容器中同时充入1.0molCO、3.0molH2O、1.0molCO2和x mol H2,则:
①当x = 5.0时,上述平衡向___________(填正反应或逆反应)方向进行。
②若要使上述反应开始时向正反应方向进行,则x应满足的条件是__________。
(3)在850℃时,若x="5.0" mol,其它物质的投料不变,当上述反应达到平衡后,求H2的体积分数(计算结果保留两位有效数字)。
I.工业上可用CO生产燃料甲醇。一定条件下发生反应:CO(g)+2H2(g) CH3OH(g)
CH3OH(g)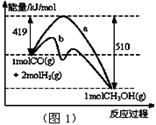
(1)“图1”表示反应中能量的变化,曲线(填“a或b”)表示使用了催化剂;该反应的热化学方程式为。
(2)若容器容积不变,下列措施可增大CO平衡转化率的是_____。
| A.升高温度 |
| B.将CH3OH(g)从体系中分离 |
| C.充入He,使体系总压强增大 |
| D.再充入1 mol CO和2 mol H2 |
(3)其他条件不变,请在“图2”中画出温度为T2(且T2<T1)时,CO的平衡转化率与H2和CO的起始组成比[n(H2)/n(CO)]的关系曲线。
II.向BaSO4沉淀中加入饱和碳酸钠溶液,充分搅拌,弃去上层清液,如此处理多次,可使BaSO4全部转化为BaCO3,发生的反应可表示为:BaSO4(s)+CO32-(aq) BaCO3(s)+SO42-(aq)。
BaCO3(s)+SO42-(aq)。
(4)现有0.20 mol BaSO4,加入1.0L 2.0mol/L的饱和Na2CO3溶液处理,假设起始的c(SO42-)≈0,平衡时,K=4.0×10-2,求达到平衡时发生转化的BaSO4的物质的量。(写出计算过程,计算结果保留2位有效数字)
某工厂废液中含有苯酚、乙酸苯酚酌,实验小组对该废液进行探究,设计如下方案:
己知熔点:乙酸16.6℃、苯酚43℃。沸点:乙酸118℃、苯酚182℃。
(1)写出②的反应化学方程式。
(2)②中分离B的操作名称是。
(3)现对物质C的性质进行实验探究,请你帮助实验小组按要求完成实验过程记录,在答题卡上填写出实验操作、预期现象和现象解释。
限选试剂:蒸馏水、稀HNO3、2moL·L-1 NaOH、0.1 mol•L-1 KSCN、酸性KMnO4溶液、FeCl3溶液、饱和浪水、紫色石蕊试液。
| 实验操作 |
预期现象 |
现象解释 |
| 步骤1:取少量C放入a试管,加入少量蒸馏水,振荡。 |
||
| 步骤:取少量C的稀溶液分装b、c两支试管,往b试管 |
产生白色沉淀 |
|
| 步骤3:往c试管 |
C与加入的试剂发生显色反应。 |
(4)称取一定量的C试样,用水溶解后全部转移至1000mL容量瓶中定容。取此溶液 25.00mL,加入KBrO3浓度为0.01667 moL·L-1的KBrO3+KBr标准溶液30.00mL,酸化并放置。待反应完全后,加入过量的KI,再用0.1100 mol•L-1Na2S2O3标准溶液滴成的I2,耗去Na2S2O3标准溶液11.80mL。则试样中C物质的量的计算表达式为:。
(部分反应离子方程式:BrO3-+5Br-+6H+=3Br2+3H2O、I2+2S2O32-=2I-+S4O62-)
工业合成氨的反应为:N2(g)+3H2(g) 2NH3(g)△H <0
2NH3(g)△H <0
某实验将3.0 mol N2(g)和4. 0 mol H2(g)充入容积为10L的密闭容器中,在温度T1下反应。测得H2的物质的量随反应时间的变化如下图所示。
(1)反应开始3min内,H2的平均反应速率为。
(2)计算该条件下合成氨反应的化学平衡常数(写出计算过程,结果保留2位有效数字)。
(3)仅改变温度为T2 ( T2小于TI)再进行实验,请在答题卡框图中画出H2的物质的量随反应时间变化的预期结果示意图。
(4)在以煤为主要原料的合成氨工业中,原料气氢气常用下述方法获得:
①C+H2O(g)  CO+H2;②CO+H2O(g)
CO+H2;②CO+H2O(g)  CO2+H2;
CO2+H2;
已知:CO(g)+1/2O2(g)=CO2(g)△H=—283.0kJ/mol
H2(g)+1/2O2(g)=H2O(g)△H=—241.8kJ/mol
写出上述CO与H2O(g)反应的热化学方程式:。
(5)合成氨工业中,原料气(N2、H2混有少量CO、NH3)在进入合成塔之前,用醋酸二氨合铜(I)溶液来吸收CO,其反应为:
CH3COO[Cu(NH3)2]+CO+NH3 CH3COO[Cu(NH3)3]•CO△H<0
CH3COO[Cu(NH3)3]•CO△H<0
写出提高CO吸收率的其中一项措施:。
亚憐酸(H3PO3)是二元酸,与足量NaOH溶液反应生成Na2HPO3。
(1)PCl3水解可制取亚磷酸:PCl3+3H2O=H3PO3+_______。
(2)H3PO3溶液中存在电离平衡:H3PO3 H++H2PO3-。
H++H2PO3-。
①某温度下,0.10mol•L-1的 H3PO3溶液 pH =1.6,即溶液中c(H+) =2.5×10-2 mol•L-1。求该温度下上述电离平衡的平衡常数K,写出计算过程。(H3PO3的第二步电离忽略不计,结果保留两位有效数字。)
②根据H3PO3的性质可推测Na2HPO3稀溶液的pH________7 (填“>”、“=”或“<”)。
(3)亚磷酸具有强还原性,可使碘水褪色。该反应的化学方程式为_______。
(4)电解Na2HPO3溶液也可得到亚鱗酸,装置示意图如下:
①阴极的电极反应式为____________________________。
②产品室中反应的离子方程式为_____________________。