甲、乙、丙、丁为四种主族元素,甲元素与乙、丙、丁三种元素相邻,甲、乙的原子序数之和等于丙的原子序数;这四种元素原子的最外层电子数之和为20。下列判断正确的是
| A.原子半径:丙>乙>甲>丁 |
| B.气态氢化物的稳定性:甲>丙 |
| C.最高价氧化物对应的水化物的酸性:丁>甲 |
| D.乙和甲或乙和丁所能形成的化合物都是剧毒物质 |
由化学能转变的热能或电能仍然是人类使用的主要能源。根据下图所示的装置,判断下列说法不正确的是
| A.该装置中Cu极为阳极 |
| B.当铜片的质量变化了12.8 g时,a极上消耗的O2在标准状况下的体积为2.24 L |
| C.该装置中b极的电极反应式是:H2+2OH--2e-===2H2O |
| D.该装置中a极为正极,发生氧化反应 |
已知:HCN(aq)与NaOH(aq)反应的ΔH="-12.1kJ/" mol;HCl(aq)与NaOH(aq)反应的ΔH="-55.6" kJ/mol,则HCN在水溶液中电离的ΔH等于
| A.+43.5 kJ/mol | B.-43.5 kJ/mol | C.-67.7kJ/mol | D.+67.7 kJ/mol |
反应2X(g)+Y(g)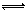 2Z(g)(正反应为放热),在不同温度(T1和T2)及压强(P1和P2)下,产物Z的物质的量n(Z)与反应时间t的关系如图所示,下述判断正确的是
2Z(g)(正反应为放热),在不同温度(T1和T2)及压强(P1和P2)下,产物Z的物质的量n(Z)与反应时间t的关系如图所示,下述判断正确的是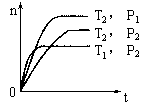

微型钮扣电池在现代生活中有广泛应用。有一种银锌电池,其电极分别是
Ag2O和Zn,电解质溶液为KOH,电极反应为:Zn+2OH--2e-=ZnO+H2O;
Ag2O+H2O+2e-=2Ag+2OH-。根据上述反应式,判断下列叙述中正确的是
| A.在使用过程中,电池负极区溶液的pH增大 |
| B.电子由Ag20极经外电路流向Zn极 |
| C.Zn是负极,Ag2O是正极 |
| D.Zn电极发生还原反应,Ag2O电极发生氧化反应 |
将pH=3的盐酸和pH=11的氨水等体积混合,完全反应后,溶液中离子浓度关系正确的是
| A.c(NH4+)>c(Cl-)>c(OH-)>c(H+) |
| B.c(NH4+)>c(Cl-)>c(H+)>c(OH-) |
| C.c(Cl-)>c(NH4+)>c(H+)>c(OH-) |
| D.c(Cl-)>c(NH4+)>c(OH-)>c(H+) |