N2O5是一种新型硝化剂,在一定温度下可发生下列反应:2N2O5(g)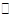 4NO2 +O2(g)△H>0,T1温度下的部分实验数据为:
4NO2 +O2(g)△H>0,T1温度下的部分实验数据为:
| t/s |
0 |
500 |
1000 |
1500 |
| c(N2O5)mol/L |
5.00 |
3.55 |
2.50 |
2.50 |
下列说法中,正确的是:
A.当反应体系内气体的平均相对分子质量不再发生变化时则该反应达到了平衡
B.T1温度下的平衡常数为K1=125,500s时N2O5的转化率为71%:
C.其他条件不变时,T2温度下反应到2000s时测得N2O5 (g)浓度为2.78mol/L, 则T1<T2
D.T1温度下的平衡常数为K1,若维持T1温度不变,增加体系压强,达到新的平衡时,平衡常数为K2,则K2>K1
下列有关金属及其化合物的说法正确的是
| A.Mg和Al都可以用电解法冶炼得到 |
| B.Na2O2、Na2O组成元素相同,与CO2反应产物也相同 |
| C.用过量的KSCN溶液除去FeCl2溶液中的少量FeCl3 |
| D.Mg和Fe在一定条件下与水反应都生成H2和对应的碱 |
已知A、B、D、E均为中学化学常见单质或化合物,它们之间的关系如图所示[部分产物略去,Fe能与足量稀HNO3反应生成Fe(NO3)3]。下列说法错误的是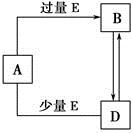
A.A、B、D可能是钠及其化合物
B.A、B、D可能是铁及其化合物
C.A、B、D可能是铝及其化合物
D.A、B、D不可能是非金属及其化合物
部分氧化的FeCu合金样品(氧化产物为Fe2O3、CuO)共5.76 g,经如下处理:
下列说法正确的是
| A.滤液A中的阳离子为Fe2+、Fe3+、H+ |
| B.样品中Fe元素的质量为2.24 g |
| C.样品中CuO的质量为4.0 g |
| D.V=896 mL |
将足量CO2通入NaOH和Ba(OH)2的混合稀溶液中,生成沉淀的物质的量(n)和通入CO2气体的体积(V)的关系如下图所示,图中AB段表示的离子方程式先后顺序正确的是
①CO2+OH-= ②CO2+2OH-=
②CO2+2OH-= +H2O
+H2O
③ +Ba2+=BaCO3↓ ④BaCO3+CO2+H2O=Ba2++2
+Ba2+=BaCO3↓ ④BaCO3+CO2+H2O=Ba2++2
⑤ +CO2+H2O=2
+CO2+H2O=2
| A.③① | B.②⑤ | C.⑤④ | D.④② |
下列实验事实所得出的相应结论合理的是
| 实验事实 |
结论 |
| A.Cl2的水溶液可以导电 |
Cl2是电解质 |
| B.将燃着的镁条伸入盛有CO2的集气瓶中继续燃烧 |
还原性:Mg>C |
| C.SO2可以使酸性KMnO4溶液褪色 |
SO2具有漂白性 |
| D.将铁粉放入稀HNO3中充分反应后,滴入KSCN溶液无明显现象 |
稀HNO3不能将Fe氧化成Fe3+ |