用NA表示阿伏加德罗常数,下列叙述中,正确的是
| A.常温常压下,5.6 g N2和CO混合物中所含有的原子总数为0.4NA |
| B.0.1 molNa2 O2中所含的阴离子数为0.2NA |
| C.将0.2 molFeCl3水解制成胶体,所得胶体粒子数为0.2 NA |
| D.标准状况下,2.24 L H2O中含有的氧原子数目为0.1 NA |
关于铅蓄电池的说法正确的是
| A.在放电时,正极发生的反应是 Pb(s) +SO42—(aq) -2e—= PbSO4(s) |
| B.在放电时,该电池的负极材料是铅板 |
| C.在充电时,电池中硫酸的浓度不断变小 |
| D.在充电时,阳极发生的反应是 PbSO4(s)+2e—=" Pb(s)+" SO42—(aq) |
可用电解法提取氯化铜废液中的铜,下列有关该实验的说法正确的是
| A.用铜片连接电源的正极,另一电极用铂片 |
| B.用碳棒连接电源的正极,另一电极用铜片 |
| C.用氢氧化钠溶液吸收阴极产物 |
| D.用带火星的木条检验阳极产物 |
β—月桂烯的结构如图所示: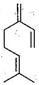 ,一分子该物质与两分子溴发生加成反应的产物(不考虑顺反异构)理论上最多有
,一分子该物质与两分子溴发生加成反应的产物(不考虑顺反异构)理论上最多有
| A.2种 | B.3种 | C.4种 | D.6种 |
在一定条件下,CO和CH4燃烧的热化学方程式分别为
2CO(g)+O2(g)===2CO2(g) ΔH=-566 kJ·mol-1
CH4(g)+2O2(g)===CO2(g)+2H2O(l) ΔH=-890 kJ·mol-1
由1 mol CO(g)和3 mol CH4(g)组成的混合气体在上述条件下充分燃烧,恢复至室温释放的热量为
| A.2912 kJ | B.2953 kJ | C.3236 kJ | D.3867 kJ |
下列有关化学反应速率和限度的说法中,不正确的是
| A.实验室用H2O2分解制O2,加入MnO2后,反应速率明显加快 |
| B.在金属钠与足量水反应中,增加水的量能加快反应速率 |
C.2SO2+O2 2SO3反应中,SO2的转化率不能达到100% 2SO3反应中,SO2的转化率不能达到100% |
| D.实验室用碳酸钙和盐酸反应制取CO2,用粉末状碳酸钙比块状反应要快 |