利用钠碱循环法可脱除烟气中的SO2。在钠碱循环法中,Na2SO3溶液作为吸收液,可由NaOH溶液吸收SO2制得。当吸收液的pH降至约为6时,需送至电解槽再生。再生示意图如下:
下列有关上述过程的说法错误的是
| A.NaOH溶液吸收SO2制得Na2SO3溶液的离子方程式:2OH-+SO2=SO32-+H2O |
| B.当吸收液呈中性时,溶液中的离子浓度满足:c(Na+)=2c(SO32-)+c(HSO3-) |
C.吸收液吸收SO2的过程中,pH与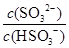 的大小成反比 的大小成反比 |
| D.HSO3-在阳极放电时的电极反应式:HSO3-+H2O-2e-=S042- +3H+ |
在温度、初始容积相同的两个密闭容器中,按不同方式投入反应物(如图所示),
发生如下反应:3 X(g)+Y(g) 2 Z(g)ΔH<0,保持温度不变,测得平衡时的有关数据如下:
2 Z(g)ΔH<0,保持温度不变,测得平衡时的有关数据如下:
| 恒容容器甲 |
恒压容器乙 |
|
| Y的物质的量/mol |
n1 |
n2 |
| Z的体积分数 |
φ1 |
φ2 |
下列说法正确的是
A.平衡时容器乙的容积一定比反应前大
B.平衡时容器甲的压强一定比反应前大
C.n2>n1
D.φ2>φ1
设NA为阿伏加德罗常数的值。下列说法正确的是
| A.将0.1 molFeCl3溶于1 L水中,所得溶液含Fe3+离子数目为0.1 NA |
| B.1 mol的羟基与1 mol的氢氧根离子所含电子数均为10NA |
| C.常温、常压下,4.6 g NO2和N2O4混合气体中含有的氧原子数目为0.2NA |
| D.在高温下,有1 mol Fe与足量的水蒸气反应,转移电子的数目为3NA |
X、Y、M、N是短周期主族元素,且原子序数依次增大。已知X的最外层电子数是电子层数的3倍,X、M同主族,Y的原子在短周期主族元素中原子半径最大。下列说法正确的是
| A.X、Y的简单离子半径:r(X2﹣)>r(Y+) |
| B.Y2X和Y2X2中阴、阳离子的个数比相同,化学键类型也完全相同 |
| C.M与X形成的化合物对应的水化物一定是强酸 |
| D.M的气态氢化物比N的气态氢化物稳定 |
实验是化学研究的基础。下列关于各实验装置的叙述正确的是
| A.装置①常用于分离互不相溶的液体混合物 |
| B.装置②可用于吸收NH3或HCl气体,并防止倒吸 |
| C.装置③可用于收集H2、CO2、Cl2、NH3等气体 |
| D.装置④可用于干燥、收集氯化氢,并吸收多余的氯化氢 |
原电池是将化学能转变为电能的装置。关于如图所示,原电池的说法正确的是
| A.Cu为负极,Zn为正极 |
| B.电子由铜片通过导线流向锌片 |
| C.溶液中H+由正极流向负极 |
| D.原电池的反应本质是氧化还原反应 |