下列说法正确的是( )
| A.增加水的浓度或温度可以加快镁跟水的反应速率 |
B.在高温密闭容器中发生反应CaCO3(s) CaO(s)+CO2(g),增加CaCO3浓度可以使反应速率加快 CaO(s)+CO2(g),增加CaCO3浓度可以使反应速率加快 |
| C.增大H2SO4的浓度,可以加快锌与H2SO4反应制取氢气的速率 |
| D.在反应S2O32-+2H+=== S↓+SO2↑+H2O中,增大S2O32-或H+的浓度可以加快硫析出的速率 |
根据图示回答,经数小时后,U形管A、B两处的液面会出现下列哪种情况(实验装置足以维持实验期间小白鼠的生命活动,瓶口密封,忽略水蒸气和温度变化对实验结果的影响) 
A、A处上升,B处下降 B、A、B两处都下降
C、A处下降,B处上升 D、A、B两处都不变
一定质量的钾、钠投入一定量的稀盐酸中,产生的气体的质量(纵轴m)随时间(横轴t)变化曲线如图:则下列说法正确的是(已知钾的还原性比钠强)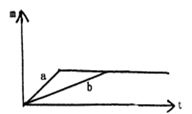
| A.曲线a为钠,曲线b为钾 |
| B.投入的Na的质量小于K的质量 |
| C.投入的Na、K的质量一定相等 |
| D.两个反应的盐酸中HCl必须足量 |
用一种试剂和必要的实验操作就能鉴别NaHCO3、NaCl、KCl、K2SO4四种物质,此试剂与实验操作是
| A.盐酸、焰色反应 | B.Ba(OH)2溶液、焰色反应 |
| C.盐酸、加热 | D.BaCl2溶液、焰色反应 |
设 表示阿伏加德罗常数,下列说法正确的是
表示阿伏加德罗常数,下列说法正确的是
A.23g钠与足量氧气充分反应,转移的电子个数为 |
B.将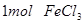 水解制成胶体,所得胶体的微粒数为 水解制成胶体,所得胶体的微粒数为 |
| C.1mol Na2O2与水完全反应时转移电子数为2NA |
| D.NA个一氧化碳分子和0.5 mol甲烷的质量比为7∶4 |
下列离子方程式书写错误的是
| A.向足量的NaHCO3溶液中逐渐滴入澄清石灰水:Ca2++2OH—+2HCO3- =2H2O+CaCO3↓+ CO32- |
| B.向足量的NaHSO4溶液中逐渐滴入Ba(HCO3)2溶液:Ba2++2H++2HCO3-+ SO42-=2H2O+BaSO4↓+2 CO2↑ |
| C.向饱和Na2CO3溶液中通入足量的CO2:CO32-+ CO2+ H2O="2" HCO3- |
| D.向NaHSO4溶液中逐渐滴入Ba(OH)2溶液至沉淀完全:H++ SO42-+ Ba2++ OH—= BaSO4↓+ H2O |