A、B、C、D均为中学化学中常见的单质或化合物,它们之间的关系如右图所示(部分产物已略去)。
(1)若A为金属单质,D是某强酸的稀溶液,则反应B+A→C的离子方程式为 。
(2)若A、B为盐,D为强碱,A的水溶液显酸性,则反应 A+D→B的离子方程式为 。
(3)若A为强碱,D为气态酸性氧化物。常温时,将B的水溶液露置于空气中,其pH随时间t变化可能如图a或图b所示(不考虑D的溶解和水的挥发)。
①若图a符合事实,则D为 (填化学式),此时图a中x 7(填“>”“<”或“=”)
②若图b符合事实,且图b中y<7,B的焰色反应为黄色,则B溶液中各离子浓度由大到小的顺序是 。
某有机物A(C8H13O2Br)在一定条件下可分别生成B1+C1和B2+C2。各物质之间的转化关系如图所示: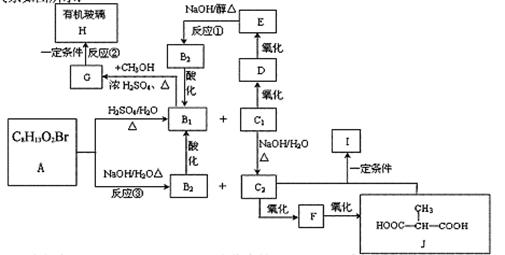
(1)C2的名称为,B1属于下列化合物中的(填序号)。
①一元醇 ②二元醇 ③卤代烃 ④醛 ⑤饱和羧酸 ⑥不饱和羧酸
(2)写出下列化学反应类型:反应①;反应②。
(3)在不同的条件下,C2和J发生化学反应可以生成多种有机物I,请写出满足下列条件的两种I的结构简式:
①C2和J按物质的量之比为1:1反应生成的最小环状化合物。
②C2和J按物质的量之比为1:1反应生成的链状高分子。
(4)写出③的化学反应方程式。
(5)满足如下条件的有机物有种(不考虑手性异构)。
①与C2相对分子质量相同;
③该物质分子中含两种不同的官能团,且Imol该物质能与金属钠反应生成1mol氢气。
(6)有机物M(C3H6O)的核磁共振氢谱显示只有一种氢,由M为有机原料也可制得有机玻璃H。请参考以下信息,写出用M和甲醇为原料(其它无机试剂任选)制备有机玻璃H的合理流程图。
有五种原子序数在36以内的元素A、B、C、D、E,它们的原子序数依次增大,A原子的最外层电子数等于其电子层数,A、B、C原子核外电子层数之和是6,C原子的电子数为A和B两元素原子电子总数的两倍;D和C的最高价氧化物对应水化物的酸性前者强于后者;E可和C形成原子个数比为1:1和1:2的两种化合物,其中一种物质是工业合成硫酸的常见原料,这两种化合物的摩尔质量相差32。试回答下列问题:
(1)E在周期表中的位置是,基态B原子的价电子排布式。
(2)写出CD2的电子式,根据价层电子对互斥(VSEPR)理论推测,CD2分子的空间构型为 ,该分子是分子(填“极性”或“非极性”)。
(3)通常情况下,AB3为无色有刺激性气味的液体,沸点303.8K,熔点193K。AB3固态时的晶体类型为;其水溶液有弱酸性,它的电离方程式为。
(4)下列性质可作为比较C、D两元素非金属性强弱依据的是(填编号)。
①C、D的最高价氧化物对应水化物的酸性强弱
②C、D的气态氢化物的水溶液的酸性强弱
③C、D的气态氢化物的稳定性强弱
④C、D的简单离子是否易被E3+氧化
⑤相同条件下,C、D的钠盐溶液的碱性强弱
合成涤纶的流程图如下所示。
回答下列问题:
(1)A的名称为;
(2) F的结构简式是;
(3) C→D的反应类型是;F→G的反应类型为;
(4)E与H反应的化学方程式为:
(5)E有多种同分异构体,符合下列条件的同分异构体有种,其中在核磁共振氢谱中出现四组峰的是(写出结构简式)。
①芳香族化合物;②红外光谱显示含有羧基;③能发生银镜反应;④能发生水解反应
(6) A也能一步转化生成E: .试剂a可以用溶液。
.试剂a可以用溶液。
芳香烃A,分子式为C3H10;某烃类衍生物X.分子式为C15H14O3,能使FeC13溶液显紫色:J分子在核磁共振氢谱中有4个特征吸收峰。在一定条件下有如下的转化关系: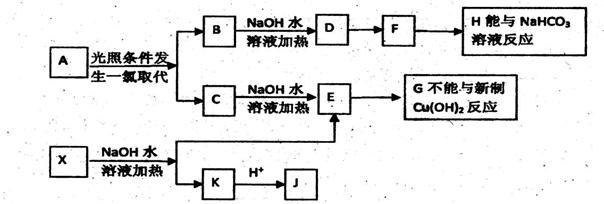
(1)A的结构简式为____,X的结构简式为。
(2)J中所含的含氧官能团的名称为____。
(3)E相H反应的化学方程式是____。
(4)向银氨溶液中滴人F发生反应的化学方程式为____。
(5)B、C的混合物在NaOH乙醇溶液中加热可以生成同一种有机能I.以I为单体合成的高分子化合物的结构简式是。
(6)已知J有多种同分异构体,试写出符合下列条件的J的同分异构体的结构简式。①与FeCl3溶液作用显紫色;②可以发生银镜反应;③苯环上只有2种不同化学环境的氢原子。
现由丙二酸和乙醛等物质合成F,合成路线如下: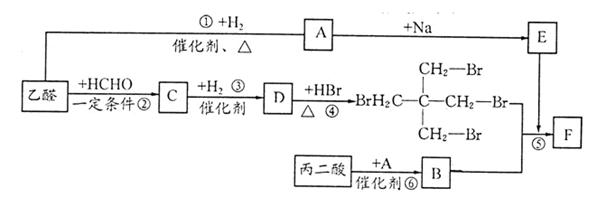

请回答下列问题:
(1)A的官能团的名称为;由逆合成分析法,推测C的结构简式。
(2)写出反应④的化学方程式;反应类型为。
(3)写出符合下列条件的D的同分异构体的结构简式。
①与D具有完全相同的官能团
②每个碳上最多只连接一个官能团
③核磁共振氢谱有5个吸收峰
(4)将E溶于酚酞稀溶液,可以观察到的现象是。已知F的质荷比最大值为384,在E的作用下合成F的化学反应方程式为。