CuSO4·5H2O是铜的重要化合物,有着广泛的应用。实验室用粗铜(含少量铁)制备CuSO4·5H2O的流程如下:
回答下列问题:
(1)实验室配制250 mL4.8 mol·L-1的稀硫酸,所需的玻璃仪器除玻璃棒、量筒、烧杯以外还需要__________________________________________________。
(2)已知不同金属离子生成氢氧化物沉淀所需的pH如下表:
| 离子 |
Fe3+ |
Cu2+ |
Fe2+ |
| 开始沉淀的pH |
2.7 |
4.4 |
7.0 |
| 沉淀完全的pH |
3.7 |
6.4 |
9.6 |
除去Fe3+,溶液的pH应控在_______________范围,调pH可选用的试剂是____________。
(3)若制得的CuSO4·5H2O中存在杂质Cu(NO3)2,进一步提纯的实验操作名称是__________。
(4)获得的CuSO4·5H2O晶体表面附着杂质离子,常用酒精洗涤的原因是____________。
用标准的BaCl2溶液测定晶体的纯度时,发现纯度大于100%(测定过程中产生的误差可忽略),其可能原因有_____________________________________________(任写一种)。
(5)实验室欲制取适量NO气体。下图中最适合的实验装置是__________(填序号),并注明装置中所需药品的名称。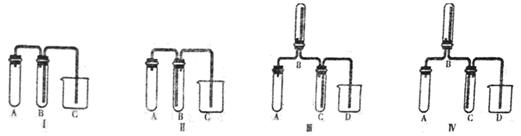
A.__________,B.__________,C.__________,D.__________。(根据选择的装置可以填满也可以不填满)
(共9分)已知NaAlO2+HCl+H2O=Al(OH)3↓+NaCl,某混合物A含有
KAl(SO4)2、Al2O3和Fe2O3,在一定条件下可实现下图所示的物质之间的变化: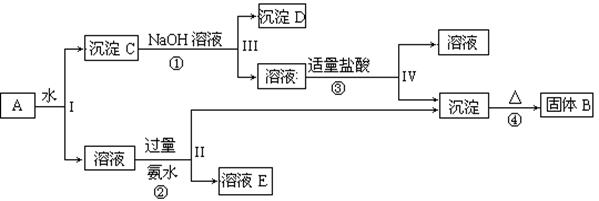 据此回答下列问题:
据此回答下列问题:
(1)I、II、III、IV四步中对于溶液和沉淀的分离采取的方法是。
(2)根据上述框图反应关系,写出下列B、D所含物质的化学式
固体B;沉淀D;
(3)写出①、②、④四个反应的化学方程式,是离子反应的写出离子方程式
①;
②;
④ 。
。
(共12分)在容积固定为2L的密闭容器中,充入0.180 molHI,480℃时反应:
2HI(g) H2(g)+I2(g),体系中n(HI)随时间变化情况如下表:
H2(g)+I2(g),体系中n(HI)随时间变化情况如下表:
| t/min |
0 |
2 |
4 |
6 |
8 |
10 |
| n(HI)/mol |
0.180 |
0.164 |
0.152 |
0.144 |
0.140 |
0.140 |
反应进行至10min后将反应混合物的温度降低,发现气体的颜色变浅。
(1)0~2min内H2的平均反应速度为。达平衡时,HI的转化率是_________。(2)上述正向反应是:反应(选填:放热、吸热)。
(3)某温度下上述反应平衡时,恒容、升高温度,原化学平衡向反应方向移动(填“正”或“逆”),正反应速率(填“增大”、“减小”或“不变”),容器内混合气体的压强(填“增大”、“减小”或“不变”)。
(4)480℃时,反应H2(g)+I2(g) 2HI(g)的平衡常数K的值为。
2HI(g)的平衡常数K的值为。
(5)要增大反应2HI(g) H2(g)+I2(g)的平衡常数,可采取的措施是(选填字母)。
H2(g)+I2(g)的平衡常数,可采取的措施是(选填字母)。
A.增大HI起始浓度
B.向混合气体中通入I2
C.使用高效催化剂
D.升高温度
某同学应用如图所示的方法研究物质的性质,其中气体a的主要成分是氯气,杂质是空气和水蒸气。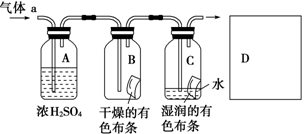
(1)该实验的主要目的是__________________________________。
(2)浓硫酸的作用是_____________________________________,
与研究目的直接相关的实验现象是________________________。
(3)从物质性质的方面来看,这样的实验设计存在着事故隐患,事故隐患表现是_____________________________________________,
请在图中D框中以图的形式表明克服事故隐患的措施
(1)Na2CO3固体中混有少量的NaHCO3固体,除去的方法是,
(2)除去铁粉中混有的少量铝粉,可选用试剂:;采取方法分离。
(3)除去FeCl2溶液中少量的FeCl3,可选用试剂。
写出离子方程式。
甲、乙两同学欲制取纯净的Fe(OH)2 ,根据如图所示的装置进行试验。A管中是Fe+H2SO4, B管中是NaOH溶液,请回答下列问题。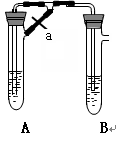
(1)同学甲:先夹紧止水夹a,使A管开始反应,在B管中观察到的现象是 。
(2)同学乙:打开a,使A管中反应一段时间再夹紧止水夹a,实验中在B管中观察到的现象是 ,B中发生反应的离子方程式为
(3)同学乙打开a的目的 ; (填甲或乙)同学可成功。