工业上用CO生产燃料甲醇。一定条件下发生反应:CO(g)+2H2(g)  CH3OH(g)。
CH3OH(g)。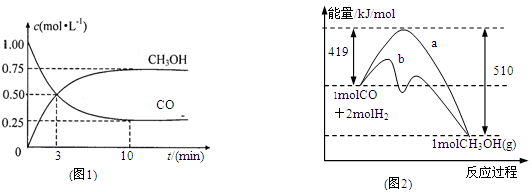
(1)图1是表示一定温度下,在体积为2L的密闭容器中加入4mol H2和一定量的CO后,CO和CH3OH(g)的浓度随时间变化情况。从反应开始到平衡,用CO浓度变化表示平均反应速率v(CO)=
(2)图2表示该反应进行过程中能量的变化。曲线a表示不使用催化剂时反应的能量变化,曲线b表示使用催化剂后的能量变化。该反应是_________(选填“吸热”或“放热”)反应,写出反应的热化学方程式 。
(3)该反应平衡常数K为______________,温度升高,平衡常数K_________(填“增大”、“不变”或“减小”)
(4)恒容条件下,下列措施中能使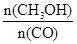 增大的有
增大的有
a.升高温度 b.充入He气
c.再充入2 molH2 d.使用催化剂
将2.80 g CaO与500 mL某浓度的盐酸充分反应,将所得溶液平均分成两份。向其中一份中加入足量的AgNO3溶液,生成的沉淀干燥后的质量为14.4 g;向另一份溶液中加入足量Zn粒,产生0.560 L(标准状况)气体。计算所用盐酸中HCl的物质的量浓度。
将某温度下的KNO3溶液200 g蒸发掉10 g水,恢复到原温度,或向其中加入10 g KNO3固体,均可使溶液达到饱和。试计算:
(1)该温度下KNO3的溶解度。
(2)原未饱和溶液中溶质的质量分数。
在标准状况下,SO2和O2混合气体500 mL,通过灼热V2O5层后,体积变为450 mL(恢复到原状况),将此450 mL气体通过足量NaOH溶液后,溶液增重0.985 g,求原混合气体中SO2的质量。