有①
②
两种貌似黄金的合金,它们都有其特殊的用途,但一些骗子常用它们做成饰品冒充真黄金欺骗消费者.对此,化学科学有责任加以揭露.
(1)现有上述两种合金制成的假黄金饰品各一件,小明同学只用稀盐酸和必要的实验仪器就鉴别出其中一种饰品是假黄金,它是合金
(2)取与上述用稀盐酸鉴别出的同种合金10
,放入烧杯中,再向其中加入93.7
某稀盐酸恰好完全反应后,测得烧杯内剩余物质的质量共为103.5
.
①上述过程中变化的质量
是
②10
,该合金中铜的质量是多少?已知反应后的溶液中溶质全部溶解,求该溶液中溶质的质量分数是多少?
已知 Na2CO3的水溶液呈碱性,在一烧杯中盛有20.4g Na2CO3和NaCl 组成的固体混合物。向其中逐渐滴加溶质质分数为10%的稀盐酸。放出气体的总质量与所滴入稀盐酸的质量关系曲线如下图所示,请根据题意回答问题: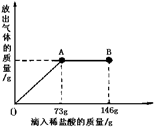
(1)当滴加稀盐酸至图中B点时,烧杯中溶液的pH7(填>、=、<)。
(2)当滴加稀盐酸至图中A点时,烧杯中为不饱和溶液(常温),通过计算求出其中溶质的质量分数。(计算结果保留一位小数)
人体缺乏维生素C(简写“Vc”)会患坏血病。右图所示为某种“维生素C”说明书的一部分,请回答:
(1)“Vc”中碳、氢、氧三种元素质量比为;
(2)若正常成人每天对“Vc”的最低需要量为60mg:当这些“Vc”完全来自右图的“维生素C”时,则每次服用“维生素C”至少片;
为了对海水中的氯化物(假设以NaCl计算)进行成分分析,甲、乙、丙三位同学分别进行实验数据如下,请仔细观察分析,回答下列问题:
| 甲 |
乙 |
丙 |
|
| 所取海水样品的质量 /g |
100 |
50 |
50 |
| 加入AgNO3溶液的质量 /g |
50 |
50 |
75 |
| 反应后所得的沉淀物的质量 /g |
1.435 |
1.435 |
1.435 |
(1)两溶液恰好完全反应的是__________的实验。
(2)请计算海水中的氯化物(以氯化钠计算)的质量分数是多少?
世界卫生组织早就把铝列为食品污染源之一,每人每日的摄入量控制在0.004g以下。若在1Kg米面食品中加入明矾2g(明矾的化学式为KAl(SO4)2·12H2O,相对分子质量为474),请回答下列问题:
(1) 人从食物中摄入的铝指的是_________(填字母)。
| A.铝元素 | B.铝单质 | C.铝合金 | D.只有明矾 |
(2) 明矾中铝元素的质量分数为(计算结果精确到0.1%)_______.
(3)如果某人一天吃了100上述米面食品,通过计算说明其摄入的铝的量是否超过安全摄入量?
电解水时,常在水中加入硫酸使反应容易进行,硫酸本身并不被分解。现用45g溶质质量分数为8%的硫酸溶液进行电解水的实验,一段时间后,溶液的质量分数为10%。计算:
(1)被电解的水的质量。
(2)电解产生氢气的质量。