向mg铁和铝的混合物中加入适量的稀硫酸,恰好完全反应生成标准状况下的气体bL。
随即向反应后的溶液中加入cmol/L氢氧化钾溶液VmL,使与硫酸反应所得的金属离子刚
好沉淀完全,并在空气中放置较长时间至沉淀不再发生改变,得到沉淀质量为ng。再将
得到的沉淀灼烧至质量不再改变为止,得到固体pg。则下列关系正确的是
| A.c=1000b/11.2V | B.p=m+(Vc/125) |
| C.n=m+17Vc | D.(10/7)m<p<(17/9)m |
下列实验“实验操作”与“结论”对应关系正确的是
| 选项 |
实验操作 |
结论 |
| A |
向Fe(NO3)2溶液的试管中加入稀H2SO4 ,在管口观察到红棕色气体 |
HNO3分解生成了NO2 |
| B |
向沸水中逐滴加入1~2 mL FeCl3饱和溶液,煮沸至红褐色液体 |
制备Fe(OH)3胶体 |
| C |
常温下,向饱和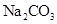 溶液中加少量 溶液中加少量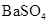 粉末,过滤,向洗净的沉淀中加稀盐酸,有气泡产生 粉末,过滤,向洗净的沉淀中加稀盐酸,有气泡产生 |
说明常温下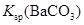 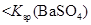 |
| D |
向纯碱中滴加足量浓盐酸,将产生的气体通入苯酚钠溶液,溶液变浑浊 |
酸性:盐酸>碳酸>苯酚 |
元素及其化合物丰富了物质世界,下列说法正确的是
| A.铜在冷的浓硫酸中会钝化,所以把铜放入冷的浓硫酸中无明显现象 |
| B.NaOH溶液和AlCl3溶液相互滴加的现象不同 |
| C.金属比非金属易失电子,所以金属可以置换非金属,而非金属不能置换金属 |
| D.Al与热水反应困难,故活泼性不及Al的金属在任何条件下均不能与H2O发生反应 |
下列有关铜锌原电池(下图)的叙述正确的是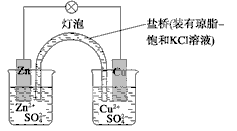
| A.正极反应为Zn-2e-===Zn2+ | B.取下盐桥,原电池仍可工作 |
| C.在外电路中,电子从正极流向负极 | D.电池反应为Zn+Cu2+===Zn2++Cu |
下列各组离子在通入SO2前后均能大量共存的是
| A.Ba2+、K+、Br-、Cl- | B.Na+、Cu2+、OH-、SiO32- |
| C.NH4+、Al3+、Br-、AlO2- | D.Li+、H+、NO3-、SO42- |
化学与生产、生活密切相关,下列说法正确的是
| A.小苏打用于治疗胃溃疡病人的胃酸过多症 |
| B.电解从海水中得到的氯化钠溶液可获得金属钠 |
| C.FeCl3溶液能与Cu反应,可用于蚀刻印刷电路板 |
| D.铝制容器不能盛放酸性或碱性食品,但可长期盛放腌制食品 |