以下是中学常见的实验装置图(图1)
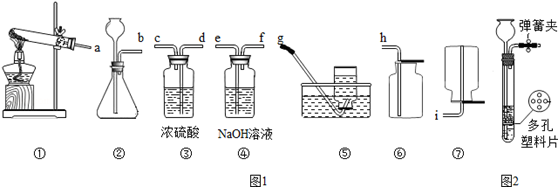
(1)实验室用锌粒和稀硫酸反应制取氢气,要制备并收集干燥的氢气,请将所选装置接口按从左到右顺序连接为.
(2)实验室制取氧气有多种方法.
a,用
制氧气应选用作为发生装置(填装置序号).检验该装置气密性的方法是.
b.如用
溶液制氧气,除
溶液外还需要加入的试剂是(填名称).如图2是实验室制备气体的一种装置图.该装置的特点是:打开弹簧夹,块状固体和液体接触,反应发生;关闭弹簧夹后,产生的气体将液面压回,使固体和液体分开,反应停止.用
溶液制氧气时,(填"可以"或"不可以")采用此装置.
c.实验室还用
来制备氧气,该反应的化学方程式为.将
与
的混合物ag加热一段时间,得到bg固体,将得到的固体溶于水,过滤、洗涤、干燥后,又得到cg固体,则
分解率为.(用含a,b.c的式子表示)(提示:
的分解率是指已分解
质量与原加入
质量之比.)
如图为某学生设计的探究可燃物燃烧条件的实验。请回答:
(1)通过此探究实验,可以说明燃烧的条件之一是什么?
(2)实验结束后,用灯帽可将酒精灯熄灭,该灭火方法的主要原理是什么?
小明把过量锌粒加入有盐酸的试管中,发现随着反应的进行,产生气体的速度逐渐加快,一段时间后逐渐减慢,最后停止产生气体。在反应过程中,溶液的温度也先随之升高,最后下降到室温。于是,小明设计实验来探究"一定质量的某种金属和同体积盐酸反应快慢的影响因素"。测得实验数据如下:某金属与同体积盐酸溶液反应实验数据表
| 盐酸溶液浓度 |
反应开始时酸 溶液的温度 |
反应开始到2分钟产生的气体体积 |
反应结束共产生气体体积 |
| 5% |
20℃ |
10 mL |
60 mL |
| 10% |
20℃ |
19 mL |
118 mL |
| 15% |
20℃ |
28 mL |
175 mL |
| 5% |
35℃ |
28 mL |
60 mL |
| 10% |
35℃ |
72 mL |
118 mL |
| 15% |
35℃ |
103 mL |
175 mL |
(1)分析实验数据得出:一定质量的某种金属和同体积盐酸反应,影响金属和酸反应快慢的主要因素有、。
(2)可以通过比较实验数据来确定金属和酸反应的快慢。
(3)过量锌粒加入盐酸中,反应开始的一段时间,反应速率逐渐加快,而不是逐渐减慢。请分析原因。。
小明家有包开启了的小苏打,久置在灶台上方,可能因受热而变质。小明为此开展了探究,请分析其过程完成填空。
【查阅资料】
①
↑
②
③
↓
④
↓
⑤
受热不分解,
、
都能溶与水。
【假设猜想】
假设一:小苏打没有变质,化学成分为
;
假设二:小苏打完全变质,化学成分为;
假设三:小苏打部分变质,化学成分为。
【实验方案】
可选药品:①
溶液 ②
溶液 ③
溶液 ④稀盐酸
| 实验操作 |
实验现象 |
实验结论 |
| 操作一:取小苏打样品少量溶于足量水后,加入过量的(填药品编号,下同),观察,如有沉淀,则继续进行下一步操作。 操作二:待操作一中反应充分后过 滤,并在滤液中加入过量的,观察。 |
操作一中无沉淀出现 |
假设一成立 |
| 假设二成立 |
||
| 假设三成立 |
【问题讨论】
有同学认为,取一定量样品直接加热,再将产生的气体通入澄清石灰水,根据实验现象,对上述三种假设的每一种是否成立都能进行判断。请评价这种方案是否合理(填"是"或"否"),理由是。
现甲、乙两化学小组安装两套如下相同装置,通过测定产生相同体积气体所用时间长短来探究影响
分解速率的因素。
(1) 下列方法能检查该装置气密性的是。
 A、将注射器活塞固定,向分液漏斗中注入适量蒸馏水,打开分液漏斗活塞,如果分液漏斗颈部能形成稳定的水柱,则气密性良好,反之气密性差。
A、将注射器活塞固定,向分液漏斗中注入适量蒸馏水,打开分液漏斗活塞,如果分液漏斗颈部能形成稳定的水柱,则气密性良好,反之气密性差。
B、关闭分液漏斗活塞,加热锥形瓶,如果注射器活塞外移(右移),停止加热后注射器活塞回到原来位置,则气密性良好,反之气密性差。
C、关闭分液漏斗活塞,用力将注射器活塞外移(右移),停止用力后,注射器活塞不移动,则气密性良好,反之气密性差。
(2)MnO2催化
下分解的化学方程式是。
(3)甲小组有如下实验设计方案,完成下表。
| 实验编号 |
实验目的 |
温度 |
催化剂 |
浓度 |
| 甲组实验Ⅰ |
探究对
分解速率的影响 |
25℃ |
二氧化锰 |
10 2% |
| 甲组实验Ⅱ |
25℃ |
二氧化锰 |
10 5% |
(4)甲、乙两小组得出如图数据。
①甲组实验得出的数据可知:浓度越大,
分解速率;
②由乙组研究的酸、碱对
分解影响因素的 数据分析:相同条件下,
在(填"酸"或"碱")性环境下放出气体速率较快;乙组提出可以用
固体与硫酸溶液反应制
(已知还生成另一种物质),其化学反应方程式为;支持这一方案的理由是。
同学们利用"硫酸、硝酸铵、氢氧化钠、碳酸钾"四种物质的溶液进行探究学习,完成下列各问:
【实验探究】
(1)
、
、
、
四组同学分别进行了下列实验.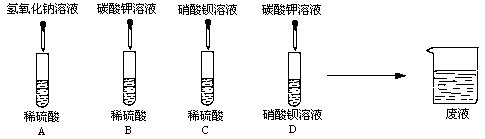
写出下列的两个化学方程式:
①
中的反应;
② 中的反应.
【挖掘实质】
下图是A组反应的微观过程示意图该化学反应的实质可以表示为
.
【实践运用】
完成试验后,四组同学将废液倒入同一个烧杯中,再将废液过滤,得到无色溶液和白色沉淀,用无色溶液滴加紫色石蕊试剂,变为红色。
(1)①溶液中的白色沉淀一定是,理由是.
(2)废液中一定不含有的离子是.
(3)为了验证该溶液中可能含有的离子是否存在,我设计如下实验进行验证
| 溶液中可能含有的离子 |
实验步骤 |
实验现象 |
实验结论 |
| 可能含有 |
②取滤液滴加 |
现象明显 |
含有该离子 |