已知:
I.
II. 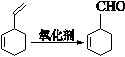
以1、3—丁二烯为有机原料,无机试剂任选,按下列途径合成甲基环己烷:
请回答:
(1)A的结构简式是 ;B的结构简式是 。
(2)写出下列反应的化学方程式:
反应① ,反应④ 。
研究NO2、SO2 、CO等大气污染气体的处理具有重要意义。
(1)利用反应6NO2+ 8NH3 7N2+12 H2O可处理NO2。当转移1.2mol电子时,消耗的NO2在标准状况下是L。
7N2+12 H2O可处理NO2。当转移1.2mol电子时,消耗的NO2在标准状况下是L。
(2)已知:2SO2(g)+O2(g) 2SO3(g) ΔH= —196.6 kJ·mol-1
2SO3(g) ΔH= —196.6 kJ·mol-1
2NO(g)+O2(g) 2NO2(g) ΔH= —113.0 kJ·mol-1
2NO2(g) ΔH= —113.0 kJ·mol-1
则反应NO2(g)+SO2(g) SO3(g)+NO(g)的ΔH=kJ·mol-1。
SO3(g)+NO(g)的ΔH=kJ·mol-1。
一定条件下,将NO2与SO2以体积比1:2置于密闭容器中发生上述反应,下列能说明反应达到平衡状态的是。
a.体系压强保持不变 b.混合气体颜色保持不变
c.SO3和NO的体积比保持不变 d.每消耗1 mol SO3的同时生成1 molNO2
测得上述反应平衡时NO2与SO2体积比为1:6,则平衡常数K=。
某混合物X由A12O3、Fe2O3、Cu、SiO2中的一种或几种物质组成。进行如下实验。
请回答:
(1)由I可知X中一定存在的是,步骤I所发生反应的离子方程式为:、。
(2)反应II的化学方程式是。
为进一步确定上述混合物X的成分,另取9.4gX进行如下实验。
(3)由Ⅲ可得出的结论为:。
(4)步骤Ⅳ所得蓝色溶液中阳离子为。
(5)原混合物中各成分的质量之比是。(不必化简)
(12分) 实验室可由软锰矿(主要成分为 MnO2)制备 KMnO4,方法如下:软锰矿与过量固体 KOH 和 KClO3在高温下反应,生成锰酸钾(K2MnO4)和 KCl;用水溶解,滤去残渣,滤液酸化后,K2MnO4转变为MnO2和 KMnO4;滤去MnO2沉淀,浓缩滤液,结晶得到深紫色的针状KMnO4请回答:
(1)软锰矿制备K2MnO4的化学方程式是。
(2)K2MnO4制备KMnO4的离子方程式是。
(3)配平氧化还原反应方程式:
__ C2O42-+__MnO4-+__H+=__CO2+__Mn2++__H2O
(4)称取6.0 g含H2C2O4·2H2O、KHC2O4和K2SO4的试样,加水溶解,配成250mL溶液。量取两份此溶液各25.00 mL,分别置于两个锥形瓶中。
①第一份溶液中加入酚酞试液,滴加0.25 mol·L-1NaOH溶液至20.00 mL时,溶液由无色变为浅红色。该溶液被中和的H+的物质的量为___mol。
②第二份溶液中滴加0.10 mol·L-1的酸性高锰酸钾溶液至16.00 mL时反应完全,此时溶液颜色由__变为__。该溶液中还原剂的物质的量为___mol。
③原试样中H2C2O4·2H2O的质量分数为_____。
(16分)铁及其化合物在生活、生产中有广泛应用。请回答下列问题:
(1)黄铁矿(FeS2)是生产硫酸和冶炼钢铁的重要原料。其中一个反应为
3FeS2+8O2 ==6SO2+Fe3O4,氧化产物为,若有3 mol FeS2参加反应,
==6SO2+Fe3O4,氧化产物为,若有3 mol FeS2参加反应,
转移mol电子。
(2)氯化铁溶液常用作印刷电路铜板腐蚀剂,反应的离子方程式为。
(3)与明矾相似,硫酸铁也可用作净水剂,其原理为(用离子方程表示)
(4)①钢铁的电化腐蚀简单示意图如右,将该图稍作修改即可成为钢铁电化学防护的简单示意图,请在下图虚线框内作出修改,并用箭头标出电子流动方向。
②写出修改前的钢铁吸氧腐蚀石墨电极的电极反应式。
(5)铁红是一种红色颜料,其成分是Fe2O.3将一定量的铁红溶于160ml5 mol·L—1盐酸中,在加入一定量铁粉恰好溶解,收集到2.24L(标准状况),经检测,溶夜中无Fe3+,则参加反应的铁粉的质量为。
(16分)对于甲、乙、丙、丁、戊五种溶液有如下信息:
①分别NH4+、Na+、Al3+、Ba2+、Ag+和NO3-、Cl-、SO42-、Br-、CO32-离子中的各一种组成(不重复)。
②其中甲、丙、戊三种溶液呈酸性,乙溶液呈碱性。
③甲、乙反应生成白色沉淀和气体,丁可分别与甲、乙、丙反应生成白色沉淀。
请回答下列问题:
⑴用化学式表示出各物质:乙、丁。
⑵请用离子方程式表示戊溶液呈酸性的原因:。
⑶请用离子方程式表示甲与乙的反应:。
⑷检验甲溶液中甲的阴离子的方法是先加试剂,再加试剂,观察到
现象,证明该阴离子存在。
⑸若丙、丁形成的白色沉淀的溶度积常数Ksp=1.8×10-20,则将1 L 1mol/L的丙溶液与1 L 1 mol/L的丁溶液混合充分反应后,不考虑溶液混合时的微小体积变化,形成沉淀的阳离子的浓度约为mol/L。