能正确描述氮原子或氮分子的化学用语是
A. |
B.1s22s22p5 | C. |
D. |
下列说法中不正确的是
| A.常温下pH=7的溶液中:Fe3+、Mg2+、SO42-、Cl-能大量共存 |
| B.在甲、乙两烧杯的溶液中,共含有Cu2+、K+、H+、Cl-、CO32-、OH-六种离子。已知甲烧杯的溶液含其中3种离子并呈蓝绿色,则乙烧杯的溶液中含有的3种离子是K+、OH-、CO32- |
| C.在含有HCO3-、SO32-、S2-、CH3COO-四种阴离子的溶液中加入足量的Na2O2固体后,CH3COO-浓度变化最小 |
| D.常温下水电离出c(H+)×c(OH-)=10-20的溶液中:Na+、ClO-、S2-、NH4+不能大量共存 |
塑化剂是一种对人体有害的物质。增塑剂DCHP可由邻苯二甲酸酐与环己醇反应制得: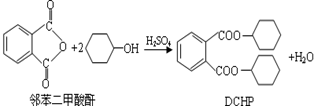
下列说法正确的是
| A.环己醇分子中所有的原子可能共平面 |
| B.1mol DCHP可与含4mol NaOH的溶液完全反应 |
| C.DCHP能发生加成、取代反应,不能发生消去反应 |
| D.DCHP易溶于水 |
液体燃料电池相比于气体燃料电池具有体积小,无需气体存储装置等优点。一种以肼(N2H4)为燃料的电池装置如图所示。该电池用空气中的氧气作为氧化剂,KOH作为电解质。下列关于该燃料电池的叙述不正确的是
| A.电流从右侧电极经过负载后流向左侧电极 |
| B.负极发生的电极反应式为:N2H4 + 4OH- - 4e - = N2+ 4H2O |
| C.该燃料电池的电极材料应采用多孔导电材料, 以提高电极反应物质在电极表面的吸附量,并使它们与电解质溶液充分接触 |
| D.该燃料电池持续放电时,正极发生氧化反应,PH减小 |
分子式为C9H10O2,能与NaHCO3溶液反应放出CO2,且苯环上一氯代物有两种的有机物有(不考虑立体异构)
| A.3种 | B.4种 | C.5种 | D.6种 |
下列有关叙述正确的是
A.在结冰路面上撒盐,是利用盐与水发生反应放出大量热,促使冰雪融化
B.蛋白质、棉花、核酸、PVC、淀粉、豆油都是由高分子组成的物质
C.利用可降解的生物质材料“玉米塑料”(主要成分为聚乳酸)替代一次性饭盒,可减少白色污染的产生
D.绿色化学的核心是利用化学原理对环境污染进行治理