化合物M是可降解的聚酯,化合物E是有机合成中间体,一种合成路线如下图所示。
完成下列填空:
(1)写出反应类型。反应①: 反应;反应②: 反应。
(2)写出结构简式。B ; M 。
(3)写出反应①的化学反应方程式 。
(4)写出检验B完全转化为C的方法。
所用试剂的化学式 ; 实验现象 。
(5)有苯环和4种不同化学环境氢原子且与E互为同分异构体的酯有 种,写出其中的一种同分异构体的结构简式 。
已知X、Y、Z、W四种元素是元素周期表中连续三个不同短周期的元素,且原子序数依次增大。X、W同主族,Y、Z为同周期的相邻元素。W原子的质子数等于Y、Z原子最外层电子数之和。Y的氢化物分子中有3个共价键。Z原子最外层电子数是次外层电子数的3倍。试推断:
(1)X、Y、Z、W四种元素的符 号:X、Y、Z、W
号:X、Y、Z、W
(2)X与Y所形成的化合物的化学式为______________,是化合物。用电子式表示其形成过程________________________ ________________。
________________。
下表列出了A~M 13种元素在周期表中的位置:
| 1 |
A |
|||||||
| 2 |
B |
C |
D |
E |
||||
| 3 |
F |
G |
H |
I |
J |
K |
||
| 4 |
L |
M |
(1)这些元素中,金属性最强的元素是_______(填元素名称,下 同),非金属性最强的是__________,最不活泼的元素
同),非金属性最强的是__________,最不活泼的元素 是_________。
是_________。
(2)写出H元素的最高价氧化物对应的水合物分别与F元素的最高价氧化物对应的水合物、J元素氢化物的水溶液反应的离子方程式_________________、。
(3)I2—、J-、L+、M2+等微粒中,半径最大的是________,最小的是__________。
(4)A与D形成的化合物A2D2是___________化合物,其电子式为_____________________。
在室温下,单质A、B、C分别为固体、黄绿色气体、无色气体,在合适的反应条件下,它们可按下面框图进行反应。又知E溶液是无色的,请回 答:
答: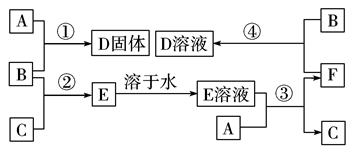
(1)写出下列物质的化学式:
A____________,B____________,C____________。
(2)反应①的化学方程式为: 。
(3)反应③的化学方程式为: 。
(4)反应④的离子方程式为: 。
已知X、Y、Z、W是短周期中的四种非金属元素,它们的原子序数依次增大,X元素的原子形成的阳离子就是一个质子,Z、W在元素周期表中处于相邻的位置,它们的单质在常温下均为无色气体,Y原子的最外层电子数是内层电子 数的2倍。
数的2倍。 试回答:
试回答:
(1) 写出下列元素的元素符号:X_________、Y_________、Z_________、 W_________。
W_________。
(2 这四种元素可组成原子个数比为5∶1∶1∶3的化合物(按X、Y、Z、W的顺序),该化合物的水溶液与足量NaOH溶液反应的离子方程式为。
(3) 将9g单质Y在足量W单质中燃烧,所得气体通入1L 1mol·L-1 NaOH溶液中,完全吸收后,将溶液在减压低温条件下蒸干,得到不含结晶水的固体质量为g。
A、B、C、D四种短周期元素,0.5molA的元素的离子得到NA个电子后被还原为中性原子;0.4gA的氧化物恰好与100mL0.2mol/L的盐酸完全反应;A元素原子核内质子数与中子数相等。B元素原子核外电子数比A元素原子核外电子数多1;Cˉ离子核外电子层数比A元素的离子核外电子层数多1;D元素原子最外层电子数是次外层电子数的2倍。请填写下列空格:
(1)推断A、B、C、D四种元素的符号A_________;B_________;C________;D________;
(2)D元素的最高价氧化物的电子式是_______________结构式该分子内含有_______键(填极性或非极性)。