镁—次氯酸盐燃料电池具有比能量高、安全方便等优点,该电池主要工作原理如图所示,其正极反应为:ClO-+H2O+2e-=Cl-+2OH-,关于该电池的叙述正确的是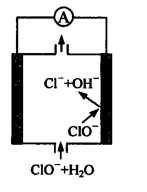
| A.该电池中镁为负极,发生还原反应 |
| B.电池工作时,OH-向正极移动 |
| C.电池工作时,正极周围溶液的pH将不断变小 |
| D.该电池的总反应式为:Mg+ClO-+H2O=Mg(OH)2↓+Cl- |
下列两种气体的分子数一定相等的是
| A.质量相等、密度不同的N2和C2H4 | B.体积相等的CO和N2 |
| C.等温、等体积的O2和N2 | D.等压、等体积的N2和C2H4 |
所谓合金,就是不同种金属(也包括一些非金属)在熔融状态下形成的一种熔合物。根据下列四种金属的熔、沸点,判断其中不能形成合金的是
| Na |
Cu |
Al |
Fe |
|
| 熔点/℃ |
97.5 |
1 083 |
660 |
1 535 |
| 沸点/℃ |
883 |
2 595 |
2 200 |
3 000 |
A.Cu和AlB.Fe和Cu C.Fe和NaD.Al和Na
同分异构现象在有机化合物中普遍存在,C4H8Cl2的同分异构体中含有2个“-CH3”的种数是
| A.2种 | B.3种 | C.4种 | D.5种 |
下列对各电解质溶液的分析正确的是
| A.向稀氨水中滴加稀盐酸至恰好中和:[NH4+]=[Cl-] |
| B.硫酸钠溶液中:[Na+]+[H+]=[OH-]+2[SO42-] |
| C.0.1mol∙L-1Na2S溶液中:[S2-]+[HS-]+[H2S]=[Na+] |
| D.向CH3COONa溶液中加适量蒸馏水:[CH3COO-]与[OH-]都减小,[OH-]/[CH3COO-]也减小 |
目前市面上有一种新型饭盒“即热饭盒”,其原理是在饭盒底部有两层,一层存放食盐水,另一层存放镁和铁的混合物,使用时打开隔离层,食物即可被快速加热。下列对其工作原理分析不正确的是
| A.打开隔层后,形成了由食盐水、镁和铁构成的原电池 |
| B.金属镁发生了氧化反应 |
| C.铁是该原电池的负极 |
| D.反应中涉及化学能、电能和热能的转化 |