写出下列化学反应方程式:
(1)溴乙烷与NaOH的乙醇溶液共热: 。
(2)将CO2通入苯酚钠溶液中: 。
(3)1,3-丁二烯的与Br2的1、4加成反应: 。
(4)葡萄糖与银氨溶液发生银镜反应: 。
芳香族化合物A有如下图的转化关系: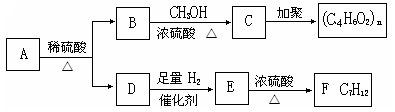
已知D能与NaOH溶液反应,E转化为F时,产物只有一种结构,且能使溴的四氯化碳溶液褪色。请回答下列问题:
(1)B的分子式是____________________________________。
(2)A、F的结构简式:A________________________F________________________
(3)写出B→C、E→F的化学反应方程式,并在括号内注明反应类型:
B→C___________________________________________________( )
E→F_______________________________________________________________
(4)符合下列3个条件的A的同分异构体有多种:
①苯环含有对二取代结构 ②遇FeCl3溶液不变色③能发生银镜反应请写出其中任意一种的结构简式____________________________
将4molO2和3molNxHy(x<y<6)的混合气体在150℃和1.05×105 Pa下点燃,完全反应后,恢复到原来的温度与压强时,测得反应后N2、O2、H2O(g)的混合气体比原混合气体的密度减少3/10。
(1)此反应的化学方程式是(用NxHy表示)___________________________
(2)x与y的关系式为___________________________________________
(3)该分子中的两个氢原子被两个甲基取代后的产物之一N可以作为火箭的主要燃料,则N的同分异构体中含碳碳单键的化合物种类共有_________________种
已知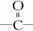 结构中,各原子与化学键共平面,—C≡C—结构中,各原子与化学键处于同一直线上,试分析如图所示的分子结构:
结构中,各原子与化学键共平面,—C≡C—结构中,各原子与化学键处于同一直线上,试分析如图所示的分子结构: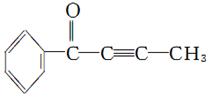
(1)该分子不能发生的反应是_______________(填序号)
①加聚反应②氧化反应③水解反应④取代反应
(2)在同一条直线上最多有________个原子
(3)能肯定在同一平面内且原子数最多的有_______个原子
(4)可能在同一平面内且原子数最多的有________个原子
(5)该分子的一种芳香族化合物同分异构体M,只有一个支链,能发生银镜反应,且醛基不与碳碳双键或碳碳三键直接相连,写出该物质与新制氢氧化铜在加热条件下的反应方程式
____________________________________________________________________________
香豆素是一种天然香料,存在于黑香豆、兰花等植物中。工业上常用水杨醛与乙酸酐在催化剂存在下加热反应制得: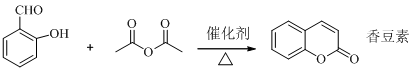
以下是由甲苯为原料生产香豆素的一种合成路线(部分反应条件及副产物已略去)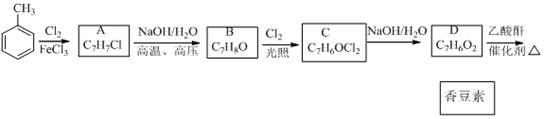
已知以下信息:① A中有五种不同化学环境的氢②B可与FeCl3溶液发生显色反应③同一个碳原子上连有两个羟基通常不稳定,易脱水形成羰基。
请回答下列问题:
(1)香豆素的分子式为 ;
(2)由甲苯生成A的反应类型为 ;A的化学名称为 ;
(3)由B生成C的化学反应方程式为 ;
(4)B的同分异构体中含有苯环的还有 种,其中在核磁共振氢谱中只出现四组峰的有 种;
(5)D的同分异构体中含有苯环的还有 种,其中:
①既能发生银镜反应,又能发生水解反应的是 (写结构简式)
②能够与饱和碳酸氢钠溶液反应放出CO2的是 (写结构简式)
有机物W-H 有如下的转化关系。已知W、B为芳香族化合物,X为卤素原子,W、A、B均能与NaHCO3溶液反应,A分子中有2个甲基,H分子中含有醛基且苯环上的取代基处于对位。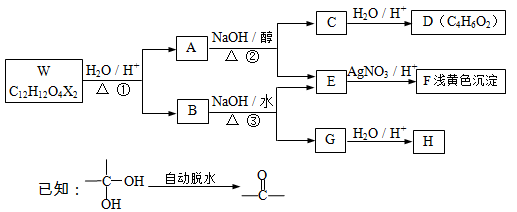
请回答下列有关问题:
(1)反应①、②分别属于 反应、 反应(填有机反应类型),A、B中均含有的含氧官能团的名称是 。
(2)F的化学式,B的结构简式。
(3)若
反应④的化学方程式是。
(4)反应②的化学方程式是。