金属钠与水的反应是中学化学中的一个重要反应。在高中化学教材的几次改版中该实验曾出现过几种不同的演示方法,分别如下图中甲、乙、丙所示: 
(1)现按图甲所示的方法,在室温时,向盛有Ca(HCO3)2溶液的水槽中,加入一小块金属钠。下列现象描述正确的是_________(填字母)。
A.钠浮在液面上,并四处游动,最后消失
B.钠熔化成一个光亮的小球
C.反应开始后,溶液由无色变红色
D.恢复到室温时,烧杯底部有固体物质析出
(2)请补充并完成甲实验中从试剂瓶中取出钠到向水槽中投入钠的有关操作:用镊子从试剂瓶中取出一小块钠→__________→用镊子夹取金属钠投入到盛有Ca(HCO3)2溶液的水槽中。
(3)按图乙所示方法来收集产生的气体,需将钠包好,再放入水中。取相同质量的钠按下列几种情况收集产生的气体在相同条件下体积最大的是 。
A.用铝箔包住钠 B.用锡箔包住钠 C.直接将钠投入的水中
(4)用装满水的矿泉水瓶按图丙方法进行实验,(用手挤压矿泉水瓶共排出水的体积为112 mL)塞紧带有钠的塞子,反应结束后,干瘪的带塞矿泉水瓶恰好恢复成原状,假设瓶内、瓶外均属于标准状况,则所用金属钠的质量是多少克?(写出计算过程)
某研究性学习小组为确定某纯净碱式碳酸镁样品的组成,设计出了下图所示的实验装置(图中A至D的部分)。[已知碱式碳酸镁Mgx(OH)y(CO3)z(x、y、z为正整数)加热能分解生成氧化镁、水和二氧化碳]
(1)按上图(夹持仪器未画出)组装好实验装置后,应首先进行的操作是__________;A处U形管盛放的药品是__________________,其作用为_______________________。
(2)指导老师在审阅设计方案后指出需要在E处增加一装置,你认为该装置应该是_____________________________.
(3)加热前需要向该装置缓缓鼓入空气数分钟,其目的是___________________;此时对活塞的操作方法是:打开活塞____________________,关闭活塞_________________。
(4)关闭活塞K1、K2,打开K3,加热一段时间后,同学们发现C处洗气瓶中几乎没有气泡冒出,这是由于_________________________。
(5)反应完全后,打开K1,再缓缓鼓入空气数分钟,其目的是_____________________。
(6)实验测得数据如下:碱式碳酸镁样品22.6 g;反应前C装置的质量为87.6 g,反应后质量为89.4 g;反应前D装置的质量为74.7 g,反应后质量为83.5 g。请计算推导该碱式碳酸镁的化学式______________________,该碱式碳酸镁受热分解的化学方程式为____________。
(共18分)某化学兴趣小组在加热下利用二氧化锰与浓盐酸反应来制取并收集氯气。
(1)制取氯气时在烧瓶中加入一定量的二氧化锰,通过(填仪器名称)向烧瓶中加入适量的浓盐酸,写出该反应的化学方程式。
(2)这种装置制取得到的氯气中可能含有少量气体和气体,若要得到纯净干燥的氯气,应使气体依次通过装有和的洗气瓶。
(3)上述反应中,氧化剂是
(4)反应结束后还可能有少量的氯气,为了防止污染空气,必须把尾气通入中,写出反应的离子方程式
(5)该小组若用200mL 10mol·L-1的浓盐酸与足量的二氧化锰固体加热反应(不考虑氯化挥发),则产生氯气的物质的量为0.5mol(填“大于”、“等于”或“小于”),原因是。
(6)87g二氧化锰与足量的浓盐酸反应,问生成的氯气在标况的体积为多少?参加反应的盐酸中被氧化的那部分的物质的量是多少?(相对原子质量:Mn—55 O—16 要求写出计算格式)
实验室用如图所示的装置制取乙酸乙酯.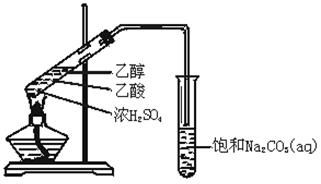
(1)在大试管中配制一定比例的乙醇、乙酸和浓硫酸的混合溶液的方法是:,然后轻轻振荡试管,使之混合均匀。
(2)装置中通蒸气的导管要插在饱和Na2CO3溶液的液面上,不能插入溶液中,目的是防止Na2CO3溶液的倒吸.造成倒吸的操作上的原因是_______________________________。
(3)浓硫酸的作用是①___________; ②___________.
(4)饱和Na2CO3溶液的作用是_______________;_________________;
_____________________________。
(5)生成的乙酸乙酯的化学方程式,乙酸乙酯的密度比水________(填“大”或“小”),有_________味.
(6)若实验中温度过高,使反应温度达到140℃左右时,副反应的主要有机产物是_____________(填物质名称).
为探究NH3的溶解性,某兴趣小组按如图所示装置进行实验(f为止水夹),请回答下列问题: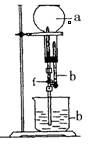
(1)写出实验室制取氨气的化学方程式。
(2)要得到干燥的氨气可选用作干燥剂。
| A.碱石灰(CaO和NaOH的混合物) | B.浓硫酸 |
| C.浓硝酸 | D.氢氧化钠溶液 |
(3)用如图装置进行喷泉实验,烧瓶中已装满干燥氨气,引发水上喷的操作是
___________________________________________.。
现用物质的量浓度为amol·L-1的标准NaOH溶液去滴定VmL盐酸的物质的量浓度,请填写下列空白:
(1)碱式滴定管用蒸馏水洗净后,接下来应该进行的操作是________________________。
(2)用标准NaOH溶液滴定时,应将标准NaOH溶液注入(选填“甲”或“乙”)中。
(3)右图是碱式滴定管中液面在滴定前后的读数,c(HCl)=_______________mol·L-1。
(4)若在滴定前滴定管尖嘴部分留有气泡,滴定后滴定管尖嘴部分气泡消失,则滴定的HCl物质的量浓度会偏____________(填“大”或“小”)。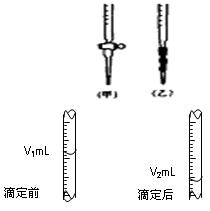
(5)取20.00 mL待测盐酸放入锥形瓶中,并滴加2~3滴酚酞作指示剂,用自己配制的标准液NaOH溶液进行滴定。重复上述滴定操作2~3次,记录数据如下。
| 实验编号 |
NaOH溶液的浓度(mol·L-1) |
滴定完成时, NaOH溶液滴入的体积(mL) |
待测盐酸的体积(mL) |
| 1 |
0.10 |
22.62 |
20.00 |
| 2 |
0.10 |
22.72 |
20.00 |
| 3 |
0.10 |
22.80 |
20.00 |
①滴定达到终点的标志是______________________________________________________。
②根据上述数据,可计算出该盐酸的浓度约为(保留两位有效数字)。