高铁酸钾(K2FeO4)是铁的一种重要化合物,具有极强的氧化性。
(1)将适量K2FeO4溶解于pH=4.74的溶液中,配制成c(FeO42-)=1.0×10-3mol·L-的试样,将试样分别置于20℃、30℃、40℃和60℃的恒温水浴中,测定c(FeO42-)随时间变化的结果如图1所示。
该实验的目的是_______________________;FeO42-发生反应的△H____________0(填“>”“<”或“=”)
(2)将适量K2FeO4分别溶解于pH=4.74、7.00、11.50的水溶液中,配制成c(FeO42-)=1.0×10-3 mol·L-的试样,静置,考察不同初始pH的水溶液对K2FeO4某种性质的影响,其变化图像见图2,800min时,在pH=11.50的溶液中,K2FeO4的浓度比在pH=4.74的溶液中高,主要原因是______________。
(3)电解法是工业上制备K2FeO4的一种方法。以铁为阳极电解氢氧化钠溶液,然后在阳极溶液中加入KOH,即在高铁酸钠溶液中加入KOH至饱和可析出高铁酸钾(K2FeO4),说明 。电解时阳极发生反应生成FeO42-,该电极反应式为______________。
(4)与MnO2—Zn电池类似,K2FeO4—Zn也可以组成高铁电池,K2FeO4在电池中作正极材料,其电极反应式为FeO42-+3eˉ+4H2O→Fe(OH)3+5OHˉ,则该电池总反应的离子方程式为_______________。图3为高铁酸钾电池和高能碱性电池放电曲线,由此可得出的高铁酸钾电池的优点有_______________________、________________________。
 (l2分)铁和铝是两种重要的金属,它们的单质及化合物有着各自的性质。
(l2分)铁和铝是两种重要的金属,它们的单质及化合物有着各自的性质。 (1)在一定温度下,氧化铁可以与一氧化碳发生下列反应:
(1)在一定温度下,氧化铁可以与一氧化碳发生下列反应: 3CO(g)+
3CO(g)+ Fe2O3(s) ⇌ 2Fe(s) +3CO2(g)
Fe2O3(s) ⇌ 2Fe(s) +3CO2(g)
 该温度下,在2L盛有
该温度下,在2L盛有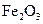 粉末的密闭容器中通入CO气体,10min后,生成了单
粉末的密闭容器中通入CO气体,10min后,生成了单 质铁11.2g。则10min内CO的平均反应速率为
质铁11.2g。则10min内CO的平均反应速率为 (2)请用上述反应中某种气体的有关物理量来说明该反应已达到平衡状态:
(2)请用上述反应中某种气体的有关物理量来说明该反应已达到平衡状态: ①②
①② (3)某些金属氧化物粉末和Al粉在镁条的引燃下可以发生铝热反应。下列反应速率(v)
(3)某些金属氧化物粉末和Al粉在镁条的引燃下可以发生铝热反应。下列反应速率(v) 和温度(T)的关系示意图中与铝热反应最接近的是。
和温度(T)的关系示意图中与铝热反应最接近的是。

 (4)写出氢氧化铝在水中发生电离的电离方程式:
(4)写出氢氧化铝在水中发生电离的电离方程式: 欲使上述体系中
欲使上述体系中 浓度增加,可加入的物质是。
浓度增加,可加入的物质是。
(l2分)一定条件下,在体积为3L的密闭容器中反 应CO(g)+2H2(g)⇌CH3OH(g)达到化学平衡状态。
应CO(g)+2H2(g)⇌CH3OH(g)达到化学平衡状态。
(1)500℃时,从反应开始到达到化学平衡状态,以H2的浓度变化表示的化学反应速率是________(用nB、tB表示)。
(2)判断该可逆反应达到化学平衡状态的标志是________(填字母)。a.v生成(CH3OH)=v消耗(CO), b. 混合气体的密度不再改变
c. 混合气体的平均相对分子质量不再改变 d. CO、H2、CH3OH的浓度均不再变化
(3)300℃时,将容器的容积压缩到原来的1/2,在其他条件不变的情况下,对平衡体系产生的影响是________(填字母)。
a. c(H2)减小b. 正反应速率加快,逆反应速率减慢,
c. CH3OH的物质的量增加 d. 重新达到平衡时,c(H2)/c(CH3OH)减小
(4) 该反应的ΔH 0(选填>、<),理由是 。
(l4分)粉末状试样A是由等物质的量的MgO和Fe2O3组成的混合物。进行如下实验:
①取适量A进行铝热反应,产物中有单质B生成;
②另取20 g A全部溶于0.2 L 6.0 mol· 盐酸中,得溶液C;
盐酸中,得溶液C;
③将①中得到的单质B和溶液C反应,有气体放出,同时生成溶液D,还残留有固体物质B。请回答:
(1)①产物中的单质B是__________________。
(2)②中所发生的各反应的化学方程式是___________________________________。
(3)③中所发生的各反应的离子方程式是_________________________________。
(4)若溶液D的体积仍视为0.2L,则该溶液中c(Mg2+)为__________________,
c(Fe2+)为___________________。
(l0分)用实验确定某酸HA是弱电解质。两同学的方案是:
甲:①称取一定质量的HA配制0.lmol/L的溶液100mL;
②用pH试纸测出该溶液的pH值,即可证明HA是弱电解质。
乙:①用已知物质的量浓度的HA溶液、盐酸,分别配制pH=l的两种酸溶液各100mL;
②分别取这两种溶液各10mL,加水稀释为100mL;
③各取相同体积的两种稀释液装入两个试管,同时加入纯度相同的锌粒,观察现象,即可证明HA是弱电解质。
(1)在两个方案的第①步中,都要用到的定量仪器是
(2)甲方案中,说明HA是弱电解质的理由是测得溶液的pH1(选填>、<、=)
乙方案中,说明HA是弱电解质的现象是(多选扣分)
(a)装HCl溶液的试管中放出H2的速率快;
(b)装HA溶液的试管中放出H2的速率快;
(c)两个试管中产生气体速率一样快。
(3)请你评价:乙方案中难以实现之处
(4)请你再提出一个合理且比较容易操作的方案(药品可任取),作简明扼要表述。
(l4分)(1)①常温下,0.01mol/L的二元酸H2A溶液的pH=5,其电离方程式为________。
②用Al 2(SO4)3与NaHCO3溶液混合反应就是泡沫灭火器的工作原理,请写出反应的离子方程式________________________________________________________。
2(SO4)3与NaHCO3溶液混合反应就是泡沫灭火器的工作原理,请写出反应的离子方程式________________________________________________________。
③比较0.1mol/L的下列各种溶液的pH大小:
CH3COONa___________NaClO;CuSO4_________KHCO3。(填“>”、“<”或“=”)
(2) 25℃ 时,如果取0.1mol/LHA溶液与0.1mol/LNaOH溶液等体积混合(忽略混合后溶液体积的变化),测得混合溶液的pH=10。试回答以下问题:
时,如果取0.1mol/LHA溶液与0.1mol/LNaOH溶液等体积混合(忽略混合后溶液体积的变化),测得混合溶液的pH=10。试回答以下问题:
①混合溶液中由水电离出的c(H+)________0.1mol/LNaOH溶液中由水电离出的c(H+);(填“>”、“<”、或“=”)
②求出混合物中下列算式的计算结果(填具体数 字):
字):
c(A-)+c(HA)=mol/L;c(OH-)-c(HA)=mol/L。