化学方程式可简明地体现元素及其化合物的性质。已知:
氧化还原反应:2FeCl3 + 2HI = 2FeCl2+ I2 + 2HCl;
2Co(OH)3 + 6HCl = 2CoCl2 + Cl2↑ + 6H2O
2FeCl2 + Cl2 = 2FeCl3
复分解反应: 2CH3COOH + K2CO3 = 2CH3COOK+ CO2 ↑ + H2O;
KCN + CO2 + H2O =" HCN" + KHCO3
热分解反应: 4NaClO △3NaCl + NaClO4;
NaClO4△NaCl + 2O2↑
下列说法不正确是( )
| A.氧化性(酸性溶液):Co(OH)3 >FeCl3 > I2 |
| B.还原性(酸性溶液):FeCl2 > HI > HCl |
| C.酸性(水溶液):CH3COOH >H2CO3 >HCN |
| D.热稳定性:NaCl>NaClO4>NaClO |
Y 元素最高正价与负价的绝对值之差是4;Y元素与M 元素形成化合物,并在水中电离出电子层结构相同的离子,该化合物是()
| A.KCl | B.Na2S | C.Na2O | D.K2S |
下列事实中,不能用于判断元素失电子能力强弱的是()
A 金属间发生的置换反应
B 金属元素的最高价氧化物对应水化物的碱性强弱
C 金属元素的单质与水或酸反应置换出氢气的难易
D 每摩尔金属单质在反应中失去电子的多少
某元素Z的核外电子数等于核内中子数,取其单质2.8 g与O2完全反应,可得6 g化合物ZO2,Z 元素在周期表中位置是()
①第3周期②第2周期③第ⅣA 族④第ⅤA族
| A.①② | B.①④ | C.①③ | D.②③ |
下列各表中的数字代表的是原子序数,表中数字所表示的元素与它们在元素周期表中的位置相符的是( )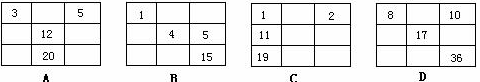
三种短周期元素A、B、C,可形成简单离子A+、B-、C2-,A、B同周期,A+ 和C2-具有相同的电子层结构。下列说法中正确的是()
A.原子序数:A>B>C B.原子核外最外层电子数:B>C>A
C.离子半径: B->A+>C2- D.原子半径: B>A>C