异丁酸苯乙醋、苯甲酸苯乙醋是常见的香料,烃A通过下列转化可得到上述有机物(已知A的相对分子质量为104,完全燃烧时生成CO2和H2O的物质的量之比为2∶1)。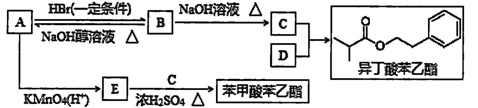
回答下列问题:
(1)A的结构简式为 。
(2)B→A的反应类型是 。
(3)D与C反应生成异丁酸苯乙酯的化学方程式为 。
(4)下列关于异丁酸苯乙酯和苯甲酸苯乙酯的说法中,不正确的是 。
a.一定条件下能发生水解反应
b.一定条件下能发生加成反应
c.等物质的量的两种有机物完全燃烧消耗等质量的O2
(5)F是苯甲酸苯乙酯的同分异构体,F属于酯类且F的二个苯环上都只有一个支链,F的结构简式为(写出其中的任意一种) 。
(6)一定条件下,由苯甲酸甲酯与苯乙醇反应也能生成苯甲酸苯乙酯。写出该反应的化学方程式: 。
火山喷发所能产生的硫磺可用于生产重要的化工原料硫酸。某企业用下图所示的工艺流程生产硫酸: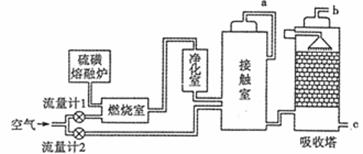
请回答下列问题:
(l)为充分利用反应放出的热量,接触室中应安装 (填设备名称)。
(2)为使硫磺充分燃烧,经流量计1通入燃烧室的氧气过量50%。为提高SO2转化率,经流量计2的氧气量为接触室中二氧化硫完全氧化时理论需氧量的2.5倍,则生产过程中流经流量计1和流量计2的空气体积比应为 ;
(3)矿物燃料的燃烧是产生大气中SO2的主要原因之一。在燃煤中加入适量的石灰石,可有效减少煤燃烧时SO2的排放,请写出此脱硫过程中反应的化学方程式 。
玻璃钢可由酚醛树脂和玻璃纤维制成。
(1)酚醛树脂由苯酚和甲醛缩聚而成,反应有大量热放出,为防止温度过高,应向已有苯酚的反应釜中缓慢加入甲醛,且反应釜应装有 装置;
(2)玻璃纤维由玻璃拉丝得到。制取普通玻璃主要反应的化学方程式为 ;
(3)玻璃钢中玻璃纤维的作用是 ;
(4)下列处理废旧热固性酚醛塑料的方法合理的是;
| A.深埋 | B.粉碎后用作树脂填料 |
| C.用作燃料 | D.用有机溶剂将其溶解,回收树脂 |
下表是甲、乙、丙、丁四种有机物的有关信息;
| 甲 |
①能使溴的四氯化碳溶液褪色;②比例模型为: ③能与水在一定条件下反应生成丙 ③能与水在一定条件下反应生成丙 |
| 乙 |
①由C、H两种元素组成;②球棍模型为 |
| 丙 |
①由C、H、O三种元素组成;②能与Na反应,但不能与NaOH溶液反应;③能与丁反应生成戊 |
| 丁 |
①由C、H、O三种元素组成;②球棍模型为 |
根据表中信息回答下列问题:
(1)写出与甲互为同系物,且比甲多一个碳原子的有机物在一定条件下生成的高分子化合物的结构简式 ;
(2)乙与液溴反应的化学方程式为 ;
(3)丙与丁反应能生成戊,戊为相对分子质量为100的酯,该反应类型为 ,其化学反应方程式为 ;(4)写出一种符合下列条件的戊的同分异构体的结构简式: ;
I.分子中不含支链并能使溴的四氯化碳溶液褪色
II.能与NaHCO3溶液发生反应
请根据表中数据回答有关问题:
| 酸或碱 |
电离常数(Ka或Kb) |
难(微)溶物 |
溶度积常数 |
| CH3COOH |
1.8×10-5 |
BaSO4 |
1×10-10 |
| HNO2 |
4.6×10-4 |
BaCO3 |
2.6×10-9 |
| HCN |
5×10-10 |
CaSO4 |
7×10-5 |
| HClO |
3×10-8 |
||
| NH3·H2O |
1.8×10-5 |
(1)表中所列四种酸中,酸性最弱的是 (用化学式表示)。下列能使醋酸溶液中CH3 COOH的电离度增大,而电离常数不变的操作是 (填序号);
A.升高温度B.加水稀释
C.加少量的CH3 COONa固体D.加少量冰醋酸
(2)已知纯水在100℃时的pH=6。该温度下0. lmol/L的NaOH溶液中,pH为 ;
(3)常温下,向水中加入少量醋酸铵固体,所得溶液呈中性,简述其原因 ;
(4)工业中制BaCl2时,需先将BaSO4转化为BaCO3。现有足量的BaSO4悬浊液,在该悬浊液中加纯碱粉末并不断搅拌,欲使SO42-物质的量浓度达到0.01 mol/L以上,则溶液中CO32-物质的量浓度应≥_______mol/L;
元素周期表中第3周期元素的单质及其化合物的用途广泛。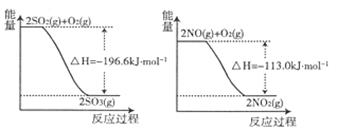
(1)该周期元素中,半径最小的简单离子的结构示意图为 ,最活泼金属元素和最活泼非金属元素形成的化合物的电子式为 ;
(2)氯的氧化物具有强氧化性,其中ClO2可将弱酸性废水中的Mn 2+转化为MnO2而除去,同时ClO2被还原为Cl--,该反应的离子方程式为 ;
(3)已知SO2,NO分别与O2反应过程中能量变化如图所示:写出NO2和SO2在一定条件下发生反应的热化学方程式 。