在容积均为500 mL的I、Ⅱ、Ⅲ三个密闭容器中分别充入l molN2和2.5 molH2,三个容器的反应温度分别为T1、T2、T3且恒定不变,在其他条件相同的情况下发生反应N2(g)+3H2(g)2NH3(g)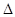 H<O。实验测得反应均进行到t min时N2的体积分数如图所示。下列说法正确的是
H<O。实验测得反应均进行到t min时N2的体积分数如图所示。下列说法正确的是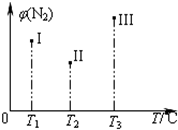
| A.当z,v(H2)=3v(N2)时,可以说明三个容器中的反应达平衡状态 |
| B.在t min时,一定达化学平衡状态的是Ⅱ和Ⅲ |
| C.在t min时,一定没有达化学平衡状态的是I |
| D.三个容器中的反应均达到平衡后,容器I中混合气体的平均相对分子质量最小 |
NA表示阿伏加德罗常数的值,下列关于 0.2mol/L K2SO4溶液的说法正确的是( )
| A.1000mL水中所含K+、SO42-总数为0.3NA |
| B.500mL溶液中含有0.2NA个K+ |
| C.1L溶液中K+的浓度为0.2mol/L |
| D.1L溶液中SO42-的浓度是0.4mol/L |
用NA表示阿伏德罗常数,下列叙述正确的是 ( )
| A.标准状况下,22.4LH2O含有的分子数为 NA |
| B.常温常压下,1.06g Na2CO3含有的Na+离子数为0.02 NA |
| C.通常状况下,NA个CO2分子占有的体积为22.4L |
| D.物质的量浓度为0.5 mol/L的MgCl2溶液中,含有Cl-个数为 NA |
实验室需用480mL0.1mol/L的硫酸铜溶液,现选取500mL容量瓶进行配制,以下操作正确的是()
| A.称取7.68g硫酸铜,加入500mL水 |
| B.称取12.0g胆矾配成500mL溶液 |
| C.称取8.0g硫酸铜,加入500mL水 |
| D.称取12.5g胆矾配成500mL溶液 |
有五瓶溶液分别是:①l0mL0.60mol•L-1 NaOH水溶液,②20mL0.50 mol•L-1H2SO4。③30mLO .4 mol•L-1 HCl④40mL0.30 mol•L-1CH3COOH水溶液,⑤50mL0.20 mol•L-1蔗糖水溶液。以上各瓶溶液所含离子、分子总数的大小顺序是
| A.①>②>③>④>⑤ | B.②>①>③>④>⑤ | C.②>③>④>①>⑤ | D.⑤>④>③>②>① |
由X、Y两元素组成的气态化合物XY4,在一定条件下完全分解为A、B两种气体物质,己知标准状况下20mLXY4分解可产生标准状况下30mL A气体(化学式为Y2)和10mL B气体,则B的化学式为
A.X2 B.Y2X2 C.XY2 D.X2Y4