在VmLFe2(SO4)3溶液中含有agFe3+,取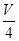 mL该溶液稀释到4VmL,则稀释后硫酸根离子的物质的量浓度是
mL该溶液稀释到4VmL,则稀释后硫酸根离子的物质的量浓度是
A.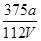 mol·L-1 mol·L-1 |
B.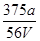 mol·L-1 mol·L-1 |
C. mol·L-1 mol·L-1 |
D.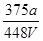 mol·L-1 mol·L-1 |
实现下列变化时,需克服相同类型作用力的是
| A.二氧化硅和干冰的熔化 | B.液溴和钠的气化 |
| C.食盐和冰的熔化 | D.纯碱和烧碱的熔化 |
处于同一周期的A、B、C、D四种短周期元素,其气态原子获得一个电子所放出的能量A>B>C>D。则下列说法中,正确的是①元素的非金属性依次增强;②元素的电负性依次减小;③元素的第一电离能依次增大;④最高价氧化物对应水化物的酸性依次减弱。
A、①④ B、②④ C、①③ D、③④
共价键、离子键和范德华力都是微粒之间的不同作用力,下列含有上述两种结合力的是
①Na2O2②SiO2③石墨④金刚石⑤NaCl ⑥白磷
| A.①②④ | B.①③⑥ | C.②④⑥ | D.③④⑤ |
能正确表示下列反应的离子方程式为
| A.漂白粉溶液在空气中失效:ClO-+CO2+H2O=HClO+HCO3- |
| B.Fe3+溶液中滴加过量的氨水: Fe3++3OH-=Fe(OH)3↓ |
| C.Cu2+溶液中滴加过量的氨水: Cu2++2NH3·H2O=Cu(OH)2↓+2NH4+ |
| D.将1mol/L NaAlO2溶液和1.5mol/L的HCl溶液等体积均匀混合: |
6AlO2-+9H++3H2O=5Al(OH)3↓+Al3+
下列有关化学用语表示正确的是
| A.二氧化硅的分子式 SiO2 | B.邻羟基苯甲酸的结构简式: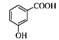 |
C.次氯酸的电子式 |
D.质子数为53,中子数为78的碘原子:131 53I |