SO2是一种重要的化工原料,也是引起酸雨污染的重要来源。
(1)某兴趣小组采用如图所示装置制取SO2
①下列实验方案适用如图所示装置制取所需SO2的试剂是_______(填序号)。
| A.Na2SO3溶液与稀硝酸 |
| B.Na2SO3固体与浓硫酸 |
| C.固体硫和氧气 |
| D.铜与浓硫酸 |
②a的仪器名称是_______。
③尾气吸收装置的连接顺序是b接( )接 ( )接e。
(2)为了回收利用SO2废气,研究人员研制了利用低品位软锰矿浆(主要成分是MnO2)吸收高温焙烧含硫废渣产生的SO2废气,制备硫酸锰晶体(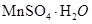 生产流程,其流程示意图如下:
生产流程,其流程示意图如下:
已知:浸出液的pH<2,其中的金属离子主要是Mn2+,还含有少量的Fe2+、Al3+等其他金属离子。有关金属离子形成氢氧化物沉淀时溶液的pH见下表:
请回答:
①含Al3+的盐常用作净水剂,用离子方程式表示其净水原理________________________。
②浸出过程中主要反应的化学方程式是___________________________________________。
③氧化过程中加入MnO2粉的目的是______________________________________________;
反应的离子方程式是_________________________________________________________。
④用石灰浆调节pH,pH应调节的范围是___________________________________。
⑤滤渣的主要成分是____________________________________。
I.有关中和滴定的操作有:①用标准溶液润洗滴定管②往滴定管内注入标准溶液③检查滴定管是否漏水④滴定⑤洗涤
正确的操作顺序是(填字母)
| A.⑤①②③④ | B.③⑤①②④ | C.⑤②③①④ | D.②①③⑤④ |
Ⅱ.氧化还原滴定实验同中和滴定类似(用已知浓度的氧化剂溶液滴定未知浓度的还原剂溶液或反之)。现有0.001mol·L-1KMnO4酸性溶液和未知浓度的无色NaHSO3溶液。反应的离子方程式是:2MnO4-+5HSO3-+H+= 2Mn2++5SO42-+3H2O
填空回答下列问题:
(1)不用(填“酸式”或“碱式”)滴定管盛放高锰酸钾溶液。
(2)选何种指示剂。(填序号)
①甲基橙②酚酞③石蕊④不用指示剂
(3)滴定前平视KMnO4液面,刻度为a mL,滴定后俯视液面刻度为b mL,则
(b-a)mL比实际消耗KMnO4溶液体积(填“多”或“少”)。根据(b-a)mL计算得到的待测液浓度,比实际浓度(填“大”或“小”)。
(4)无论是KMnO4溶液往NaHSO3溶液中滴,还是NaHSO3溶液往KMnO4溶液中滴,在其他操作正确规范的前提下,下列操作一定会使测定结果偏高的是。(填序号)
①取用NaHSO3溶液的滴定管未用待测NaHSO3溶液润洗
②取用KMnO4酸性溶液的滴定管未用标准KMnO4酸性溶液润洗
③滴定过程中不慎有液体溅出
④滴定前仰视读数,滴定后平视读数
为测定放置已久的小苏打样品中纯碱的质量分数,设计如下实验方案:
(1)方案一:称取一定质量的样品,置于坩埚中加热至恒重后,冷却,称取剩余固体质量,计算。实验中加热至恒重的目的是。
(2)方案二:按下图装置进行实验。并回答以下问题。
①实验前先_______________。分液漏斗中应该装_____(盐酸或硫酸)。D装置的作用是。
②实验中除称量样品质量外,还需称___________装置前后质量的变化。
③根据此实验得到的数据,测定结果有误差。因为实验装置还存在一个明显缺陷,该缺陷是。
(3)方案三:称取一定量样品,置于小烧杯中,加适量水溶解,向小烧杯中加入足量氯化钡溶液。过滤、洗涤,干燥沉淀,称量固体质量,计算:
①过滤操作中,除了烧杯外还用到的玻璃仪器有_______________;
②实验中判断沉淀是否完全的方法是。
③如加入试剂改为氢氧化钡,已知称得样品9.5g,干燥的沉淀质量为19.7g,则样品中碳酸钠的质量分数为____________(计算结果保留两位有效数字)。
(8分)有一乡村中学由于条件有限,仅有一大一小两种试管和稀硫酸。甲、乙两个学生找来铝或废牙膏皮,各自设计了一种装置,制取并收集一试管氢气。(如图)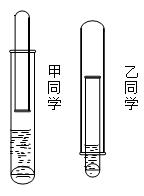
(1)哪个学生设计的装置比较合理?。另一个装置不合理的原因(至少说出一个原因)。
(2)用较合理的装置制取氢气,要使氢气充满收集氢气的试管,应该采取的措施是。
(3)还可以用哪些物品代替牙膏皮和稀硫酸完成制取氢气的实验?
。
已知乙二酸(HOOC―COOH,可简写为H2C2O4)俗称草酸,易溶于水,属于二元中强酸(为弱电解质),且酸性强于碳酸,其熔点为101.5℃,在157℃升华。某校研究性学习小组为探究草酸的部分化学性质,进行了如下实验:
(1)向盛有1 mL饱和NaHCO3溶液的试管中加入足量乙二酸溶液,观察到有无色气泡产生。该反应的离子方程式为_________________________________________________。
(2)向盛有少量乙二酸饱和溶液的试管中滴入用硫酸酸化的KMnO4溶液,振荡,发现其溶液的紫红色褪去,说明乙二酸具有_________________(填“氧化性”、“还原性”或“酸性”),请配平该反应的离子方程式:
____ MnO4– + ____ H2C2O4 + _____ H+ =" _____" Mn2+ + _____ CO2↑ + _____ H2O
(3)将一定量的乙二酸放于试管中,按下图所示装置进行实验(夹持装置未标出):
实验发现,装置C、G中澄清石灰水变浑浊,B中CuSO4粉末变蓝,F中CuO粉末变红,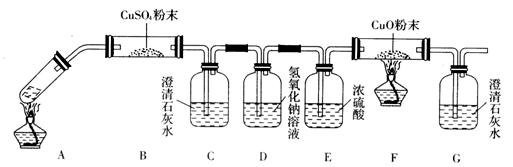
据此,乙二酸分解的产物为______________________。上述装置中,D的作用是______。装置F中发生反应的化学方程式为: _________________________________________。
(4)该小组同学将2.52g草酸晶体(H2C2O4•2H2O)加入到100 mL 0.2 mol/L的NaOH溶液中充分反应,测得反应后溶液呈酸性,其原因是_________________________________。
某学习小组从海带中提取I2,实验步骤如下:
(1)实验室焙烧海带,需要下列仪器中的____________
a.试管 b.烧杯 c.坩埚 d.泥三角 e.铁三角架 f.酒精灯
(2)将所得海带灰加水溶解、过滤,所需玻璃仪器有_______________________________
(3)在滤液中检出了I-,还检出了K+,检验K+的操作步骤是_______________________。
(4)经查阅资料,得知氧化性由强到弱的顺序为:Cl2 > IO3- > H2O2 > I2,他们决定用H2O2做氧化剂氧化KI,而不用Cl2,原因可能是____________________________。
(5)小组用CCl4萃取碘水中的碘,在如图的分液漏斗中,下层液体呈_______色;打开分液漏斗活塞,却未见液体流下,原因可能是___________。
(6)根据以下数据推测:
①已知SiCl4的沸点是57.6℃,则CCl4的沸点_________(填“高”或“低”)于57.6℃
②已知I2的沸点是113.6℃,熔点是185.2℃,从碘的CCl4溶液中分离出碘单质,应采取的方法是___________。
| A.过滤 | B.升华 | C.蒸发 | D.蒸馏 |