下列变化过程中,属于还原反应的是
| A.HCl→Cl2 | B.Na→Na+ | C.CO→CO2 | D.Fe3+→Fe |
某酸性溶液中只有Na+、CH3COO-、H+、OH-四种离子。则下列描述正确的是()
| A.该溶液由pH=3的CH3COOH与pH=11的NaOH溶液等体积混合而成 |
| B.该溶液由等物质的量浓度、等体积的NaOH溶液和CH3COOH溶液混合而成 |
| C.加入适量NaOH,溶液中离子浓度为c(CH3COO-)>c(Na+)>c(OH-)>c(H+) |
| D.加入适量氨水,c(CH3COO-)一定大于c(Na+)、c(NH4+)之和 |
室温下,将0.100 0 mol·L-1盐酸滴入20.00 mL 未知浓度的某一元碱MOH溶液中,溶液pH随加入盐酸体积变化曲线如图所示。下列有关说法不正确的是()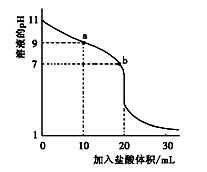
| A.b点:c(M+)+c(MOH)=c(Clˉ) |
| B.a到b点的水溶液导电性依次增强 |
| C.该一元碱溶液浓度为0.100 0 mol·L-1 |
| D.室温下,MOH的电离常数Kb=1×10-5 |
相同条件下,现有四种溶液:①pH=2的CH3COOH溶液;②pH=2的HCl溶液;③pH=12的氨水;④pH=12的NaOH溶液。下列有关说法正确的是()
| A.由水电离出的c(H+):①=②=③=④ |
| B.将②、③溶液混合后,pH=7,消耗溶液的体积:③>② |
| C.等体积的①、②、④溶液分别与足量铝粉反应,②生成的H2的物质的量最大 |
| D.向溶液中加入100mL水后,溶液的pH:③>④>①>② |
pH=1的无色溶液中,可大量共存的一组离子是()
| A.Fe3+、Na+、NO3-、SO42- | B.Cu2+、NH4+、SO42-、CO32- |
| C.Ba2+、Na+、Cl-、ClO- | D.Al3+、K+、NO3-、Cl- |
一定温度下,某NaCl稀溶液中c(H+)为1×10-6 mol·L-1,下列说法正确的是()
| A.该NaCl溶液显酸性 | B.该NaCl溶液中Kw=1×10-14 |
| C.该NaCl溶液稀释10倍后pH=7 | D.该NaCl溶液中Kw=1×10-12 |