某有机化合物3.2 g在氧气中充分燃烧只生成CO2和H2O,将生成物依次通入盛有浓硫酸的洗气瓶和盛有碱石灰的干燥管,实验测得装有浓硫酸的洗气瓶增重3.6 g,盛有碱石灰的干燥管增重4.4 g。则下列判断正确的是
| A.只含碳、氢两种元素 |
| B.肯定含有碳、氢、氧三种元素 |
| C.肯定含有碳、氢元素,可能含有氧元素 |
| D.根据题目条件可求出该有机物的最简式,无法求出该有机物的分子式 |
高温下,某反应达平衡,平衡常数K=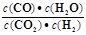 .恒容时,温度升高,H2浓度减小。下列说法正确的是
.恒容时,温度升高,H2浓度减小。下列说法正确的是
| A.该反应的焓变为正值 |
| B.恒温恒容下,增大压强,H2浓度一定减小 |
| C.升高温度,逆反应速率减小 |
| D.该反应化学方程式为CO+H2O=CO2+H2 |
在相同温度和压强下,对反应CO2(g)+H2(g) CO(g)+H2O(g)进行甲、乙、丙、丁四组实验,实验起始时放入容器内各组分的物质的量见下表
CO(g)+H2O(g)进行甲、乙、丙、丁四组实验,实验起始时放入容器内各组分的物质的量见下表
 |
CO2 |
H2 |
CO |
H2O |
| 甲 |
amol |
amol |
0mol |
0mol |
| 乙 |
2amol |
amol |
0mol |
0mol |
| 丙 |
0mol |
0mol |
amol |
amol |
| 丁 |
amol |
0mol |
amol |
amol |
上述四种情况达到平衡后,n(CO)的大小顺序是
A.乙=丁>丙=甲 B.乙>丁>甲>丙
C.丁>乙>丙=甲 D.丁>丙>乙>甲
一定温度下,可逆反应A2(s)+3B2(g) 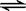 2AB3(g)达到平衡的标志是
2AB3(g)达到平衡的标志是
| A.容器内每减少1mol A2,同时生成2mol AB3 |
| B.容器内每减少1mol A2,同时消耗3mol B2 |
| C.混合气体总的物质的量 |
| D.密闭容器内的物质的质量不再改变 |
在容积固定的密闭容器中存在如下反应: A(g)+3B(g) 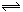 2C(g)该反应正反应为放热反应。某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,并根据实验数据作出下列关系图:下列判断一定错误的是
2C(g)该反应正反应为放热反应。某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,并根据实验数据作出下列关系图:下列判断一定错误的是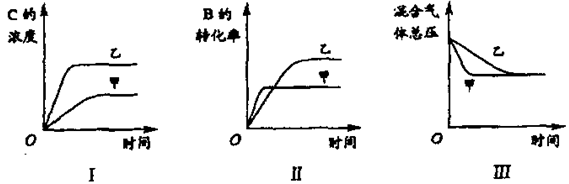
| A.图Ⅱ研究的是温度对反应的影响,且甲的温度较高 |
| B.图Ⅲ研究的是不同催化剂对反应的影响,且甲使用的催化剂效率较高 |
| C.图I研究的是不同催化剂对反应的影响,且乙使用的催化剂效率较高 |
| D.图I研究的是压强对反应的影响,且乙的压强较高. |
甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是
①CH3OH(g)+H2O(g)=CO2(g)+3H2(g);△H= +49.0 kJ·mol-1
②CH3OH(g)+1/2O2(g)=CO2(g)+2H2(g);△H= -192.9 kJ·mol-1
下列说法正确的是
| A.CH3OH的燃烧热为192.9 kJ·mol-1 |
B.反应①中的能量变化如图所示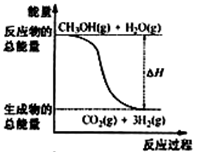 |
| C.CH3OH转变成H2的过程一定要吸收能量 |
| D.根据②推知反应: CH3OH(l)+1/2O2(g)=CO2(g)+2H2(g)的△H>-192.9kJ·mol-1 |