氢气是一种清洁能源,氢气的制取与储存是氢能源利用领域的研究热点。
(1)以甲烷为原料制取氢气是工业上常用的制氢方法。已知:
CH4(g)+H2O(g) ===CO(g)+3H2(g) ΔH=+206.2 kJ/mol
CH4(g)+CO2(g) ===2CO(g)+2H2(g) ΔH=+247.4 kJ/mol
CH4(g)与H2O(g)反应生成CO2(g)和H2(g)的热化学方程式为 。
(2)硫铁矿(FeS2)燃烧产生的SO2通过下列碘循环工艺过程既能制H2SO4,又能制H2。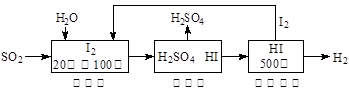
已知1g FeS2完全燃烧放出7.1 kJ热量,FeS2燃烧反应的热化学方程式为 。
该循环工艺过程的总反应方程式为 。
(3)电解尿素[CO(NH2)2]的碱性溶液制氢的装置示意图见图(电解池中隔膜仅阻止气体通过,阴、阳极均为惰性电极)。电解时,阳极的电极反应式为 。
(4)用吸收H2后的稀土储氢合金作为电池负极材料(用MH表示),NiO(OH)作为电池正极材料,KOH溶液作为电解质溶液,可制得高容量,长寿命的镍氢电池。电池充放电时的总反应为:
NiO(OH)+MH Ni(OH)2+M
Ni(OH)2+M
①电池放电时,正极的电极反应式为 。
②充电完成时,Ni(OH)2全部转化为NiO(OH)。若继续充电将在一个电极产生O2,O2扩散到另一个电极发生电极反应被消耗,从而避免产生的气体引起电池爆炸,此时,阴极的电极反应式为 。
(5)Mg2Cu是一种储氢合金。350℃时,Mg2Cu与H2反应,生成MgCu2和仅含一种金属元素的氢化物(其中氢的质量分数为0.077)。Mg2Cu与H2反应的化学方程式为 。
(8分)实验室里迅速制备少量氯气可利用以下反应:
2 KMnO4+16 HCl ="==" 2 KCl + 2 MnCl2 + 5 Cl2↑ + 8 H2O
此反应不需要加热,常温下就可以迅速进行,而且对盐酸的浓度要求不高。
(1)该反应中,氧化剂是__________,还原剂是_________。
(2) 当电子转移的数目为6.02×1023个时生成的氯气的物质的量为 mol
mol
(⑶被氧化的还原剂的物质的量是 mol
mol
写出符合以下离子方程式的化学方程式各1个
(1)CO2+2OH-=CO32-+H2O __________________________________________
(2)HCO3-+H+=CO2↑+H2O _________________________________________
_________________________________________
(3)CaCO3+2H+=Ca2++CO2↑+H20 _________________________________________
(4)Zn+Cu2+=Zn2++Cu_________________________________________
(5)H++OH-=H2O _________________________________________
除去括号中杂质,写出所加试剂与反应的离子方程式。
⑴SO42-(CO32-),所加试剂:_________,离子方程式:___________________________。
⑵Cl-(SO42-),所加试剂:_________,离子方程式:___________________________。 ⑶Fe2+(Cu2+),所加试
⑶Fe2+(Cu2+),所加试 剂:_________,离子方程式:___________________________。
剂:_________,离子方程式:___________________________。
⑷NO3-(Cl-),所加试剂:_________,离子方程式:___________________________。
某溶液中可能大量存在下列阴离子中的一种或几种:SO42-、CO32-、CL-。
⑴当溶液中有大量H+存在时,则不可能大量存在。 ⑵当溶液中有大量Ba2+存在时,则不可能大量存在和
⑵当溶液中有大量Ba2+存在时,则不可能大量存在和
⑶当溶液中同时有大量Ba2+和存在时,上述阴离子都不可能大量存在。
李比希曾用下列装置测定有机物中碳、氢含量。现称取a mg有机物样品利用该装置进行碳、 氢含量测定,最终发现盛有高氯酸镁的吸收管增重b mg,盛有碱石棉的吸收管增重c mg。
氢含量测定,最终发现盛有高氯酸镁的吸收管增重b mg,盛有碱石棉的吸收管增重c mg。
试回答:
(1)a mg有机物样品应置于该装置中处(填序号,(2)同);
(2) 加热时,应先加热处,后加热处;
(3) 装置中氧 化铜的作用是;高氯酸镁的作用是
化铜的作用是;高氯酸镁的作用是 ;碱石棉的作用是。
;碱石棉的作用是。
(4) 该有机物中碳的质量分数为;氢的质量分数为。